2020年在CASP13中成为基准,AlphaFold排名第一;随后赢得CASP14,其预测结构可达到原子精度;
2021年底,AlphaFold2预测全人类蛋白质并开源数据库,Nature将其列入年度十大科学事件。
今日,AlphaFold在分子生物学界再掀波澜。
01、从全人类到整个地球
7月28日,DeepMind公司与欧洲生物信息研究所(EMBL-EBI)团队联合公布:AlphaFold预测出含植物、细菌、真菌在内的100万个物种,2.14亿个蛋白质结构,几乎涵盖了地球上所有已知蛋白质。
在超2亿个蛋白质结构预测结果中,约35%具有高精度,达到了实验手段获取的结构精度;80%的结构足以用于多项后续分析。
这一重大飞跃,再次引爆学术界。
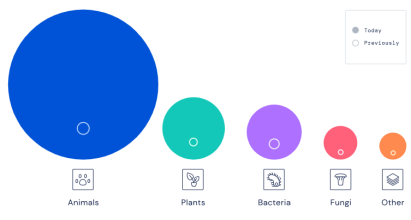
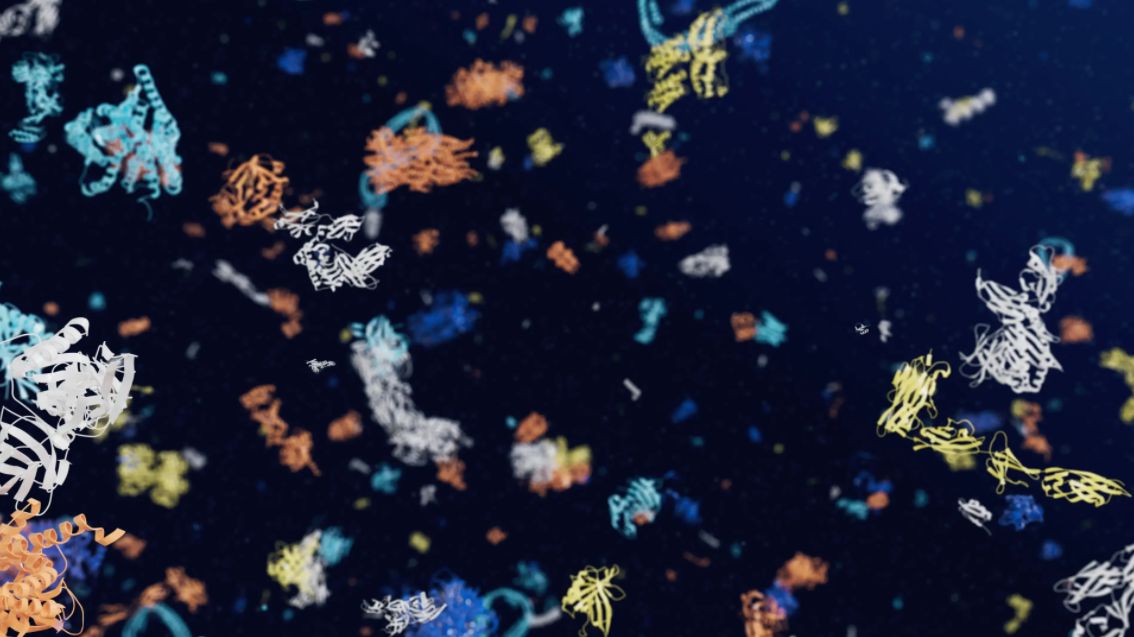
图:AlphaFold此次预测的蛋白质结构,涵盖大量动植物及微生物物种
目前,含2亿多个蛋白质结构的数据库已免费公开,并将通过Google Cloud Public Datasets提供批量下载。
这是我们给全人类的一份礼物,DeepMind创始人Demis Hassabis在推特上激动地表示,“以后查找蛋白质结构,会像使用搜索引擎一样简单”。
接下来,研究团队还将继续开发预测蛋白质折叠方式的算法模型,伦敦大学学院Tomek Wlodarski 博士指出。
在过去一年里,有关AlphaFold结构研究的科学文章高达上千篇,产业界也纷纷展开行动。
02、改变了游戏规则
DeepMind表示,迄今为止已经有来自190个国家的50多万名研究人员访问了AlphaFold数据库,查看超过200万个结构。
此外,还有AlphaFold 的“超级用户”:研究人员在自己的服务器上安装了软件,或者转向基于云的 AlphaFold 版本来预测不在 EMBL-EBI 数据库中的结构,或者为该工具设想新用途.
Nature调查显示,自AlphaFold开源以来,学术界(包括发表论文和预印本)对其的引用大幅上升。
图:AlphaFold开源后学界论文的引用数量(含预印本)
“AlphaFold 改变了游戏规则”,有科学家称。
科学家已经逐步运用其解析蛋白质结构、识别新的蛋白质种类、预测蛋白质相互作用、以及运用其预测和探索人类未知的蛋白物质。当然,AlphaFold的预测并不是完全准确,还需要通过实验室对结果进行验证。
除了蛋白质结构预测外,人工智能工具也在被用来设计全新的蛋白质,以及基于结构设计药物。例如曾在AlphaFold2开源前一个月,发明RoseTTAFold的Dvid Baker课题组,已从蛋白质结构预测逐渐转型为蛋白质设计。
他们的最新研究结果表明,只根据靶点结构即可实现从头设计结合特定位点,甚至特定功能的结合蛋白。
随着AI技术的突破以及相关应用的成熟,国内与蛋白质药物/基于结构设计的初创公司也获得资本青睐。
据智药局此前统计,仅今年二季度,全球有超8起融资蛋白质药物/蛋白质组学/基于结构设计药物相关融资。包括已开发多种蛋白药物设计与建模的创新算法华深智药,蛋白质结构预测及设计的分子之心和智峪生科、AI+蛋白质组学络米生命科技等。
此前DeepMind决定将AlphaFold运用到实际的药物研发中来,推出子公司Isomorphic Labs,以及和DNDi(被忽视疾病药物研发倡议组织)合作,共同致力于寻找治疗被忽视疾病的药物,比如恰加斯病和利什曼病。
DeepMind称,他们已经迫不及待地想看到AlphaFold2接下来会对世界各地的科学家产生怎样的影响。
从了解疾病到保护蜜蜂,到破译生物难题,再到更深入地研究生命本身的起源,一切都皆有可能。
参考链接:
https://www.nature.com/articles/d41586-022-00997-5
https://www.ebi.ac.uk/about/news/technology-and-innovation/alphafold-200-million/
内容中包含的图片若涉及版权问题,请及时与我们联系删除




评论
沙发等你来抢