不同种类细胞中基因组构象的差异决定了基因表达的特异性,进而决定不同细胞类型的功能差异。长久以来,从原位杂交到高通量检测如 Hi-C、micro-C 技术,基因组构象检测的实验方法通常耗时耗力、成本高昂且有很强的技术局限性。这些方法极大地限制了这些实验技术在基因组构象研究领域的广泛应用,尤其是研究稀有细胞类型以及需要大规模验证基因组构象调控的因果关系等方面。这些方法的局限性也长期限制三维基因组构象调控领域里的新发现。
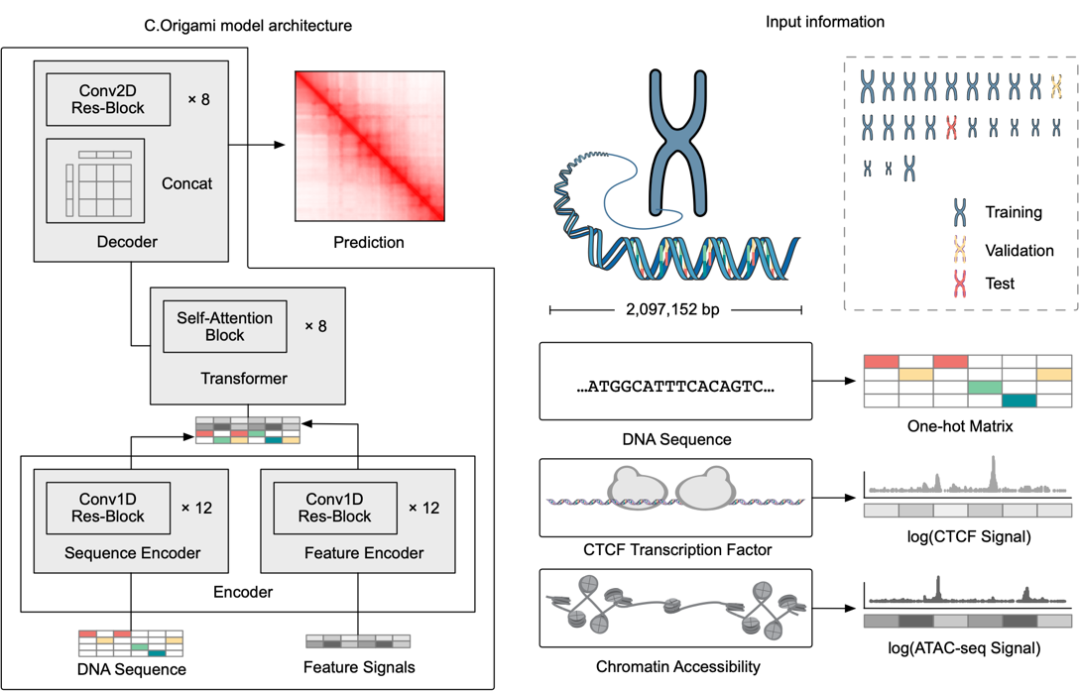
图 1
2023 年 1 月 9 日,纽约大学医学院(NYU Grossman School of Medicine)Aristotelis Tsirigos 实验室和博德研究所(Broad Institute of MIT and Harvard)夏波实验室合作在 Nature Biotechnology 上发表文章《Cell type-specific prediction of 3D chromatin organization enables high-throughput in silico genetic screening》。

论文地址:https://www.nature.com/articles/s41587-022-01612-8
这项研究中,第一作者纽约大学医学院博士生谭济民与夏波博士首先提出了新型多模态机器学习模型 C.Origami 来预测特定细胞类型的染色质构象,并基于遗传筛选的原理提出了全新的高通量计算遗传筛选 (in silico genetic screening, ISGS) 方法,用以鉴定细胞类型特异性的功能基因组元件,助力发现新的染色质构象调控机理。
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢