
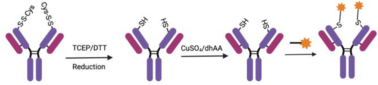
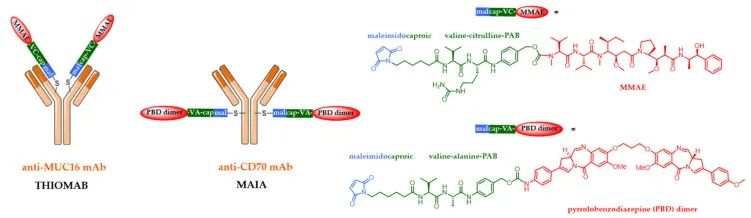
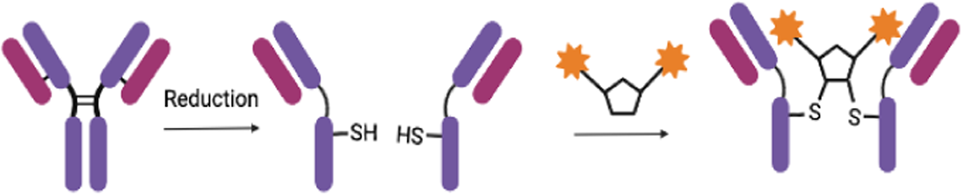
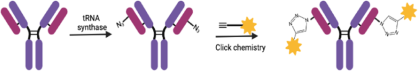
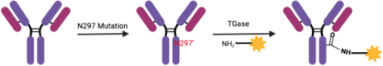
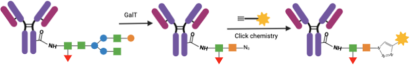
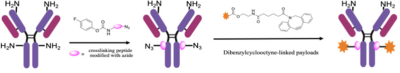
ADC药物偶联,指将ADC各组分连接起来的连接方式,决定药物抗体偶联比(DAR)和均一性,影响药物的活性、耐受性和稳定性,一般分为随机偶联和定点偶联两类。非定点偶联常见的方式为Lys残基偶联和Cys残基偶联。定点偶联,则包括引入反应性半胱氨酸、二硫键重桥、非天然氨基酸技术、酶催化技术、糖基偶联技术和临近诱导抗体偶联(pClick)技术。定点偶联因其DAR值更易控制,产出的ADC药物均一性好,已成为偶联方法的研发趋势。智药局以此为切入点,就定点偶联六大技术各自优缺点进行介绍,并以相关公司技术为例,展开深度分析。引入反应性半胱氨酸,又名 Thiomab 技术,最早由基因泰克开发。简单来说,就是通过基因工程在抗体的特定点插入半胱氨酸残基,然后将半胱氨酸上的羟基和毒素偶联,形成位点专一的抗体偶联药物。Thiomab 技术,工程化引入半胱氨酸,既不会干扰免疫球蛋白的折叠和组装,也不会改变抗体抗原的结合模式,获得的ADC药物既保留了其体内抗肿瘤活性,还提高了耐受性、降低了系统毒性。该技术具有高均一性、较好的反应活性和稳定性等优点,缺点是需要基因修饰,通常DAR 2。目前,罗氏靶向CD79b的ADC产品Iladatuzumab vedotin(DCDS0780A),采用的就是 Thiomab 技术。基于此,Seattle Genetics 和 Spirogen 开发了一种类似的技术,称为 MAIA,通过在 mAb 关键区域的 239 位引入丝氨酸-半胱氨酸突变,用于其 PBD 二聚体的生物缀合。二硫键重桥,又名 Disulfide re-bridging,是利用半胱氨酸选择性交联试剂(如TECP或DTT),将IgG1抗体中4个链间二硫键还原,随后使用双反应试剂在多肽链重新连接的同时,完成小分子有效载荷的安装或抗体的进一步修饰。通过共价重新连接半胱氨酸残基,既维持了二硫键的稳定作用,同时实现每个二硫键链接一个有效载荷的受控偶联。该偶联方式具有高均一性、不影响抗体的空间结构、通用的氨基酸序列与糖基化修饰等优点,缺点是链内错误桥接,通常DAR 4。Lgenica Biotherapeutics的SNAP平台和Abzena的Thiobridge平台使用了二硫键还原改造的技术。非天然氨基酸技术,顾名思义,通过在抗体的原始序列中人工加入非天然氨基酸,使其在抗体表面呈现出可方便偶联的特异性位点,从而获得位点确定、DAR值均一的ADC。该偶联技术独特之处在于可以随意突变非天然氨基酸,并且得到任意DAR值的ADC,缺点是需要基因修饰、抗体表达量低、非天然氨基酸序列引起免疫原性和非天然氨基酸的疏水性引起聚集。Ambrx 公司的 ARX788 是首个利用非天然氨基酸开发的抗体偶联药物,目前正寻求上市申请。ARX788 选择的非天然氨基酸是乙酰苯丙氨酸(pAF),pAF上的酮基可与有效载荷AS269上的羟胺基团形成肟键,发生特异性位点的偶联,产生均质的ADC。同样采用非天然氨基酸联偶技术得还有STRO-002,是Sutro开发靶向FRα并拥有全球知识产权的第三代ADC。该药抗体部分合成过程采用无细胞蛋白质合成技术(XpressCF),该技术可在蛋白质特定位点嵌入非天然氨基酸,所得抗体的非天然氨基酸可以通过点击化学反应定点引入cathepsin B可裂解连接子,实现ADC定点偶联。酶催化技术,通过在抗体序列中插入可以被一些专门酶识别的特定氨基酸标志物,使得毒素可以与抗体有选择性的进行连接。该技术可以选择位点,DAR值可选择,但需要基因改造来插入酶识别序列,且有外来氨基酸序列引起的免疫原性的风险。在我国,启德医药是较早以差异性的酶催化定点偶联技术开发ADC药物的创新高科技企业之一。与传统的化学偶联方式不同,启德医药基于多年合成生物学领域的积累,差异性地开发了两套独特的基于生物酶催化定点偶联技术体系iLDC和iGDC,分别通过转肽酶和糖基转移酶工程化改造实现了高度均质ADC药物的制备。公司旗下的 GQ1001 就是根据其独特的连接酶催化偶联技术和拥有专利的开环连接子技术,通过毒素DM1与曲妥珠单抗的定点特异性偶联产生的ADC。此外,石药集团的 SYS6002 通过采用其专有的酶催化定点抗体偶联技术,能将有效的有丝分裂抑制剂 MMAE 针对性地导向 Nectin-4 表达的癌细胞,而其连接子的稳定性有助于将高浓度的 MMAE 送达肿瘤中,并同时通过减少不良的全身暴露量而将副作用减低。糖基偶联技术,通过用糖苷内切酶修饰天然蛋白质中不同的糖基,曝露出N-乙酰氨基葡萄糖,然后经过叠氮化学修饰后的N-乙酰半乳糖胺利用糖基转移酶连接到抗体的N-乙酰氨基葡萄糖上,最后发生点击化学反应可以得到定点偶联的ADC。该技术优点在于药物连接子与糖链偶联,而不改变氨基酸序列,并且它们连接在远离氨基酸残基的地方。但该方法需要糖工程所需的特殊试剂和酶。如在修饰过程中的试剂有引入外源因子风险的,其纯化工艺应充分考虑外源因子的去除,并参考ICH Q5A开展病毒清除研究。Syniffix的核心平台GlycoConnect™,就是基于糖基化的定点偶联技术平台。GlycoConnect™,通过将有效载荷锚定到抗体的 N297的聚糖上,实现高效的定点偶联。通过对每个 N-聚糖进行糖苷内切酶修饰和精确的一个叠氮化物标记,引入了一个独特的锚点,用于与有效负载的无铜点击反应偶联。糖岭生物的糖基化偶联技术叫“DisacLink”技术,只用一种酶,反应时间短,偶联率高且稳定。该技术不仅极大地缩减了定点ADC药物制备的复杂工艺,降低了定点ADC药物研发成本,而且可以兼容不同的药物及连接子结构,实现定点ADC化合物的结构多样性制备,为候选药物筛选提供了丰富的结构多样性。pClick技术,通过引入邻近激活交联剂,叠氮基修饰的肽可以自发地与抗体上最接近的赖氨酸残基反应。叠氮基团为具有生物正交手柄修饰有效负载的点击化学提供了可用位点。pClick技术无需对抗体进行任何改造,而是将毒素-连接子与抗体亲和蛋白相连,然后让抗体亲和蛋白再与抗体进行临近诱导反应,从而获得任意DAR值的ADC分子。此外,该技术可在温和条件下将有效载荷定点附着到天然抗体上,从而最大限度地减少与抗原受体或fcriii受体(负责激活抗体依赖性细胞介导的细胞毒性的受体)结合的干扰。pClick 技术为 ADC 开发提供了一种新的选择,以更方便、更高效的方式进行定点偶联。https://www.nature.com/articles/s41392-022-00947-7/tables/2



内容中包含的图片若涉及版权问题,请及时与我们联系删除
























评论
沙发等你来抢