

关于AI制药,一个很经典的叙事角度常常被提起:
小分子化合物空间拥有10的60次方,而AI能够帮助我们最大探索化合物空间。
不过,研发一款药物真的有必要探索到10的60次方吗?要知道,人类很快就能学会使用经验或者其他方法来简化问题。
举个例子,当我们需要外出吃饭,整个城市有2000家餐馆可供选择,但如果只要10分钟路程能够到达的餐馆,那么可选择的数量大大降低,这就叫降维。
而就算是AI的加入,使用全球的算力,也不可能一下子全部探索10的60次方的化合物空间。
那么如何判断一家AI制药公司的技术平台和资产?
一家公司的资产是源于对药物发现过程的理解。药物发现过程的核心在于用专门开发的测试方法对化合物库进行筛选。
一家公司的资产既要用其化合物库的广度和深度,也要运用技术与化合物库相结合来发现有前景的药物。
也就是说,人工智能和药物发现的进展将需要解决低维问题,或同时采用在提高数据质量的同时降低问题维数的方法。
在知名投行Stifel看来,AI赋能药物研发,降维的过程主要有三种方式。
 基于物理第一性原理的方法
基于物理第一性原理的方法
在人工智能出现之前,基于物理的第一性原理计算是CADD(计算机辅助药物发现)的核心方法。
简单来说,就是使用传统方法生成一系列先导化合物。然后使用基于物理学的第一原理进行筛选,以确定具有良好药物特性的靶标新药。
例如,应用物理学意味着运行分子动力学模拟来计算分子在水中的溶解度,或分子对特定蛋白质的亲和力,或其渗透性。
这种方式的重点是了解结合位点的化学性质和物理性质,非常适合寻找针对x射线或低温电镜晶体结构存在的目标的药物。
有哪些公司在做这些事情?包括薛定谔、Relay,国内的公司也包括晶泰科技、深势科技、腾迈医药、予路乾行等。
薛定谔
上述公司中又以薛定谔的计算化学方法最被大众所熟知。薛定谔主要使用原子力场数据和自由能扰动(FEP+)来筛选可能具有药物性质的化合物。

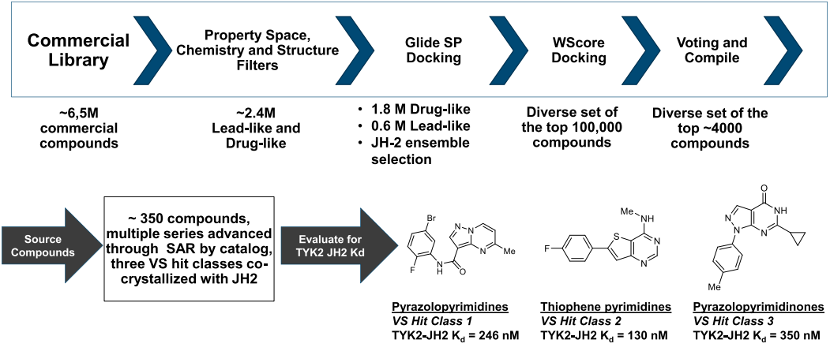
一个经典的案例是,薛定谔和Nimbus的合作中,通过x射线共晶结构,建立了一个基于结构的大型化合物库,使用大规模的FEP+物理模型发现了TYK2抑制剂。
2022年12月24日,武田以60亿美元的价格收购Nimbus Therapeutics的全资子公司Nimbus Lakshmi, Inc.及其TYK2抑制剂NDI-034858,预付款为40亿美元。
晶泰科技
晶泰科技的三位创始人都是麻省理工的物理学博士,因此晶泰科技也将大规模物理学模型也用于药物发现。
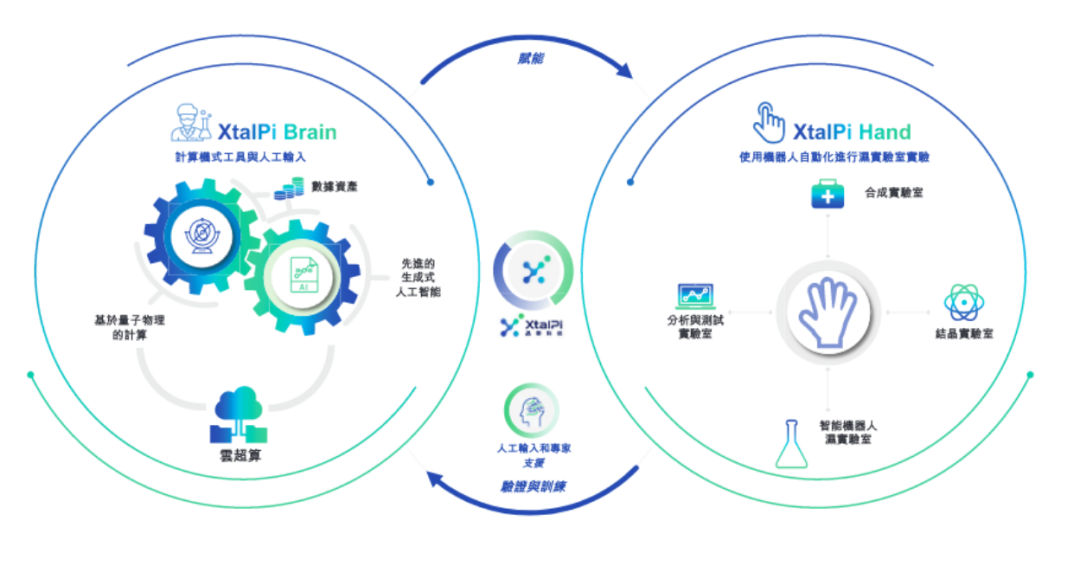
在和辉瑞的合作中,晶泰科技帮助新冠口服药的开发,晶泰科技的数字预测算法和实验验证。研究小组仅用了6周时间就完成了药物晶体结构预测与实验结果的相互验证和精确匹配,为后续的研发和生产提供了可能。
 采用QSAR + 机器学习方法
采用QSAR + 机器学习方法
以上方法适用于有准确的靶点结构,但很多时候研发人员没有这样的信息,于是就出现了QSAR + 机器学习的方法。
生成一系列候选药物,并使用高通量分析研究它们的结合和性质。然后使用机器学习方法将这些分析结果与药物结构相关联,以识别药效团的结构活性关系。使用机器推荐的新化学结构来迭代寻找具有良好结合、特异性和特性的药物。
这种技术非常适合于晶体结构不存在的情况下,仍然希望找到一个好的结合分子,但不太适合药物靶标未知的情况。
Kimia
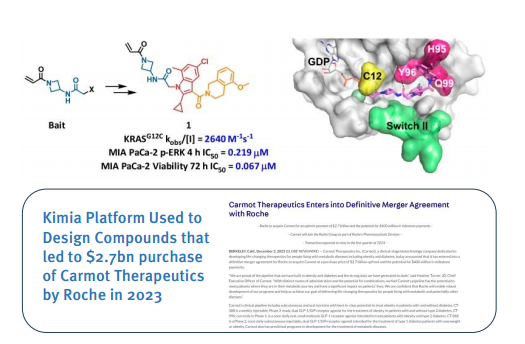
其中的代表公司包括则是Kimia。Kimia是由Carmot拆分的一家公司,2023年12月,罗氏以31亿美元收购Carmot。
Kimia可以通过自动化学合成和筛选结合主动学习算法,快速探索与目标生物分子结合的化合物的大化学空间。
然后使用化学合成、分析数据(QSAR)、ADME数据等来训练一个主动学习模型,该模型预测下一轮文库合成和筛选的化合物。这是一个迭代过程,一直持续到确定候选药物为止。
而Kimia前身公司,Carmot使用其化学演化和QSAR方法生成安进的LUMAKRAS®,整个筛选是在细胞中针对已知或新的(未知)靶标进行的生化筛选。
除此之外,LabGenius使用迭代类QSAR方法进行抗体设计,通过合成生物学、机器人自动化和ML领域的技术,该平台能够智能地发现新的治疗性蛋白质。

 基于细胞扰动
基于细胞扰动
首先,找到与疾病目标相关的组织特异性细胞模型。然后对细胞进行广泛的药物干预。收集使用转录组学(RNAseq)或其他输出的数据。
这种方法非常适合生物学复杂或未知的环境。如果存在与疾病相关的细胞,则可以在不知道靶标的情况下研究候选药物的效果。
这些以细胞为基础的公司最有可能在涉及复杂生物学的领域取得突破,并提高对蛋白质/疾病途径的理解。
使用这种方法的公司包括insitro、Anima、Genetech、immunia、Vevo等,不过最为著名的是上市AI制药公司Recursion。
Recursion
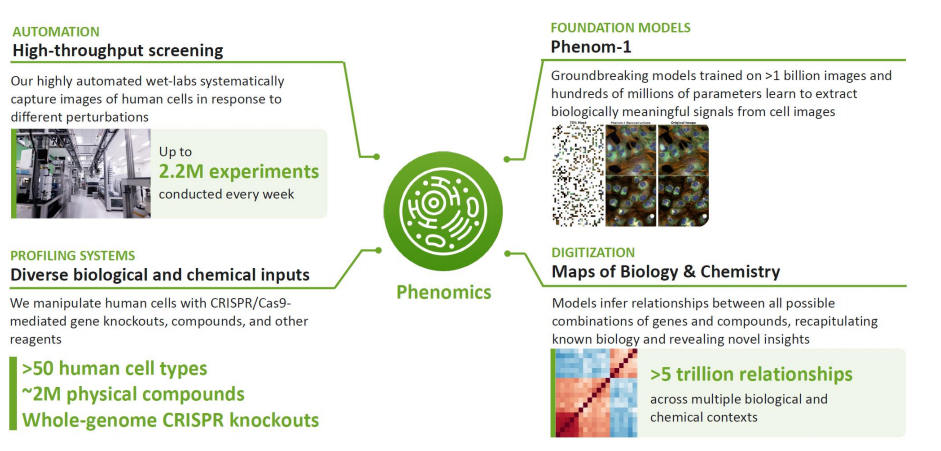
Recursion将高内涵显微镜技术与阵列式CRISPR基因组编辑技术相结合,可以在多种人类细胞环境中描绘庞大的、高维的生物和化学扰动库,以创建人类生物学的数字“图谱”。
目前,Recursion已经拥有庞大的专有生物和化学数据集,超过23PB和3万亿可搜索基因和化合物关系。
经过多年的数据清洗训练,其以细胞图像为最主要的数据集已有巨大的竞争优势。2023年5月,英伟达宣布以5000万美元投资Recursion,获得其4%的股份。
Eikon
由诺贝尔化学奖Eric Betzig博士创办,Eikon成立以来已经融资7.75 亿美元,可以说是一家biotech独角兽。
Eikon最重要的就是其超分辨率荧光显微技术,而Eric Betzig博士正是通过这项发明获得了2014年的诺贝尔化学奖。
运用超分辨率显微镜实时观察细胞中蛋白质的运动,结合机器学习和生物工程,进而开发治疗癌症等严重疾病的创新药物。他们已经可以将观察尺度缩小到10纳米,观测周期缩短至10微秒。
写在最后
事实上,不止以上三种方法,更多公司是使用复合型技术的公司,CADD和AIDD的技术边界已经逐渐变得模糊。
不过,对于一家AI制药公司而言,最难攻克的仍然是拥有高质量的生物学和化学关系数据库,清洗外部数据变得繁琐而低效,许多公司正在利用“干湿实验循环”构建内部数据库。
更重要的是,我们不仅需要看到公司怎样理解和筛选化合物,还有生成的药物分子。
也就是说,不仅是母鸡,更重要的是看到金蛋。
从这方面的结果来看,真正将人工智能模型整合到实验性药物设计和发现管线,现在还为时过早。
—The End—
推荐阅读

内容中包含的图片若涉及版权问题,请及时与我们联系删除





评论
沙发等你来抢