DRUGONE
设想一下这样的情景:到了 2040 年,药物研发效率显著提升,得益于能够在计算机上进行虚拟细胞的模拟实验。研究人员借助 AI 模拟的细胞模型,在实验室操作之前,就能预测药物、基因变化或环境刺激带来的影响,从而节省时间、减少花费,甚至拯救生命。
什么是“虚拟细胞”?

它是通过人工智能构建的,能够在计算机中模拟活细胞的核心结构与行为的数字模型。研究者们认为:
“我们真正理解一个细胞的全部——从分子结构、功能、细胞间作用机制,到对任何干预的反应——将极大助力于治愈、预防和控制疾病。”
—— Patricia Brennan,Chan Zuckerberg Initiative 科技与科学总经理

技术发展脉络:从观察到模拟
此项技术的发展历经多个阶段:
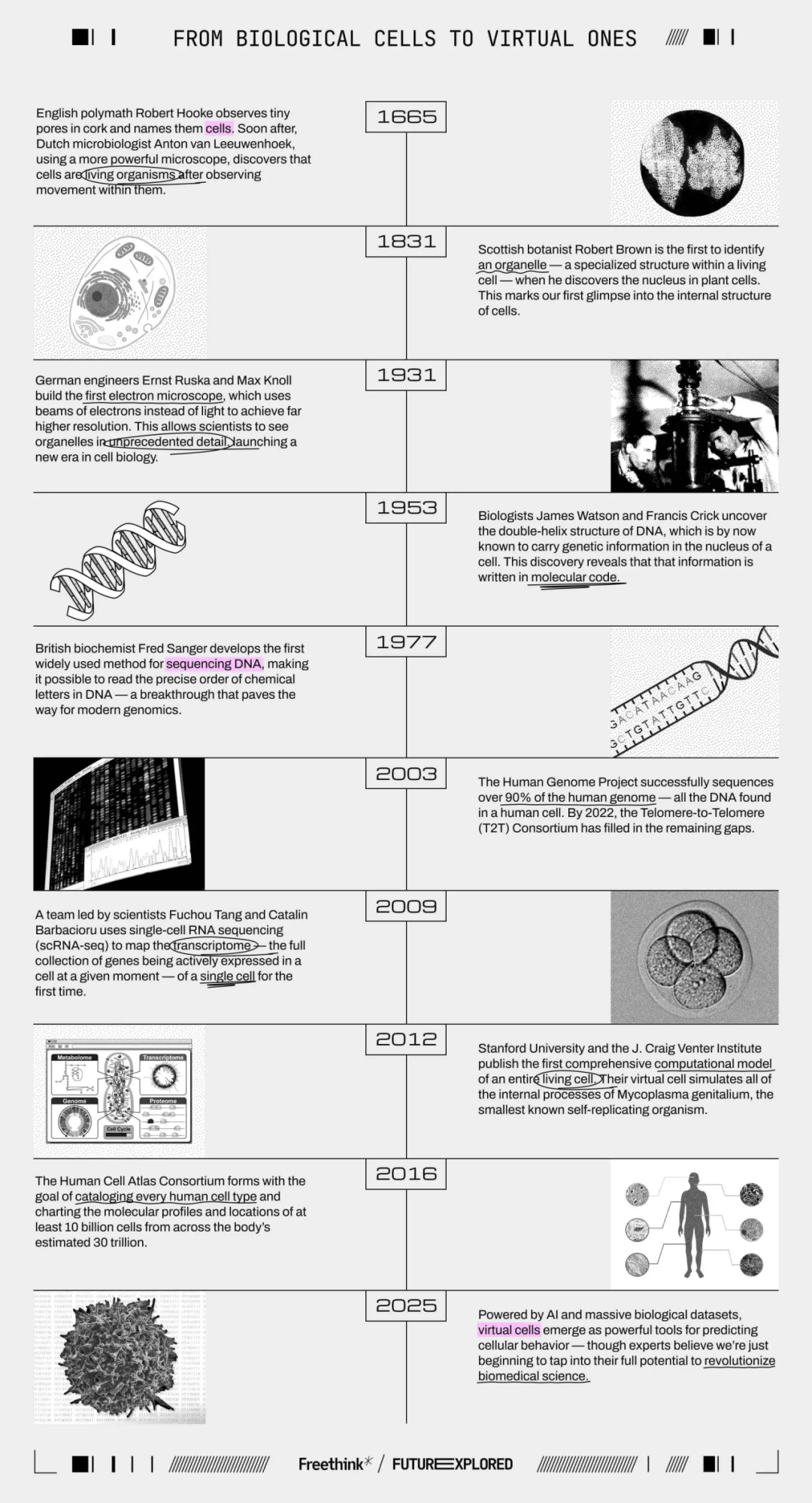
17 世纪以来,显微镜让我们第一次观察到“细胞”;之后不断推动对细胞结构、功能的理解,比如发现细胞核、发明电子显微镜、揭示 DNA 双螺旋结构等。
进入 21 世纪后,人们开始用数学方程和代码试图模拟细胞模型——比如模拟细菌的整个生命周期。如今,更先进的 AI 技术(如大型语言模型、transformer 架构)正在被用来捕捉更复杂的生物学关系。
为什么现在有机会?
实现这一愿景的契机主要来自以下三方面:
数据的海量积累:各种测序技术、显微成像、单细胞多组学等方法,让我们掌握了前所未有的大规模生物学数据。
AI 算力与算法突破:AlphaFold 模型对蛋白质结构预测的成功表明,通过 AI 可以辅助解决关键生物难题;这为虚拟细胞的发展打下坚实基础。
跨领域协作与平台建设:像 Chan Zuckerberg Initiative(CZI)这样的机构正在构建开放数据平台,让学术界、企业界齐聚一堂,共同推进模型训练与验证。

前沿进展与新进展
Foundation 模型构建:研究者尝试开发能预测 DNA、RNA、蛋白质等的通用模型——类似语言模型在 AI 中的地位,未来它们可能成为生物学领域的“一体化语言”。
专家质疑与理性讨论:并非所有人都看好这种“一体化”的方法。约翰斯·霍普金斯大学的 Salzberg 指出,通用模型可能比不上专用于蛋白质折叠的 AlphaFold,更缺乏针对特定问题的精准性。
赛博智能代理系统(CellForge):2025 年 8 月的一项重大突破中,研究团队提出了 CellForge——一个能自主从原始单细胞多组学数据与任务说明中,生成建模策略与训练代码的多智能体系统,用于模拟虚拟细胞。实际测试表明,该系统在预测基因扰动、药物处理与细胞刺激等方面表现优异。

当前挑战:数据与整合的复杂性
虽然已有多样化数据来源(基因组、蛋白质、显微图像等),但仍缺乏能够动态模拟细胞如何随时间变化的数据,这对模拟扰动响应至关重要。
不同模型的整合仍是难题 :怎样把 DNA/RNA/蛋白质/细胞行为模型拼接成完整、协调运作的虚拟细胞?这需要跨学科合作与设计标准—同时也考验着可解释性与模型验证策略。

展望未来:机会与应用
如果实现,虚拟细胞可用于药物筛选、突变效应预测、个性化治疗方案测试,大幅加速实验节奏、提高成功率。
另一个重大前瞻是建立类似 AlphaFold 在蛋白领域的“foundation model”,但面向更高层次的生命系统——这或将彻底颠覆医学研究逻辑,让发现更多由计算主导,人类更专注验证。
同时,围绕模型的伦理、安全与可解释性必须同步推进。毕竟,生物模拟的误差直接关系患者安全。
整理 | DrugOne团队
参考资料
https://www.freethink.com/artificial-intelligence/virtual-cells

内容为【DrugOne】公众号原创|转载请注明来
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢