
近日,诺贝尔化学奖得主David Baker团队发表了一篇预印版论文《Computational design of pH-sensitive binders》,介绍了他们如何通过计算手段设计pH敏感性蛋白质。本文将为您深入解读这篇论文,并分享编者的一些思考。
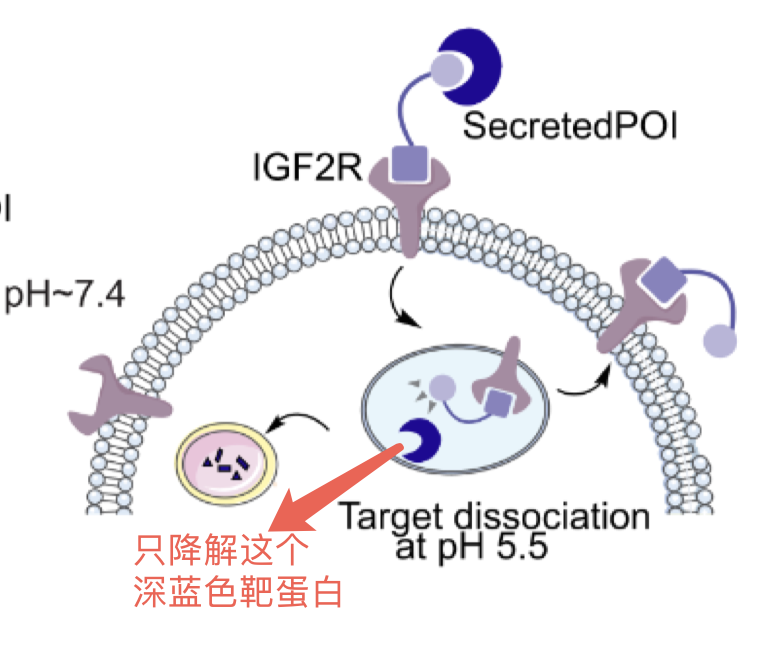
动态的pH梯度是真核细胞生物学的基础,在各种生物微环境中都涉及到PH的变化,pH变化无处不在。比如:
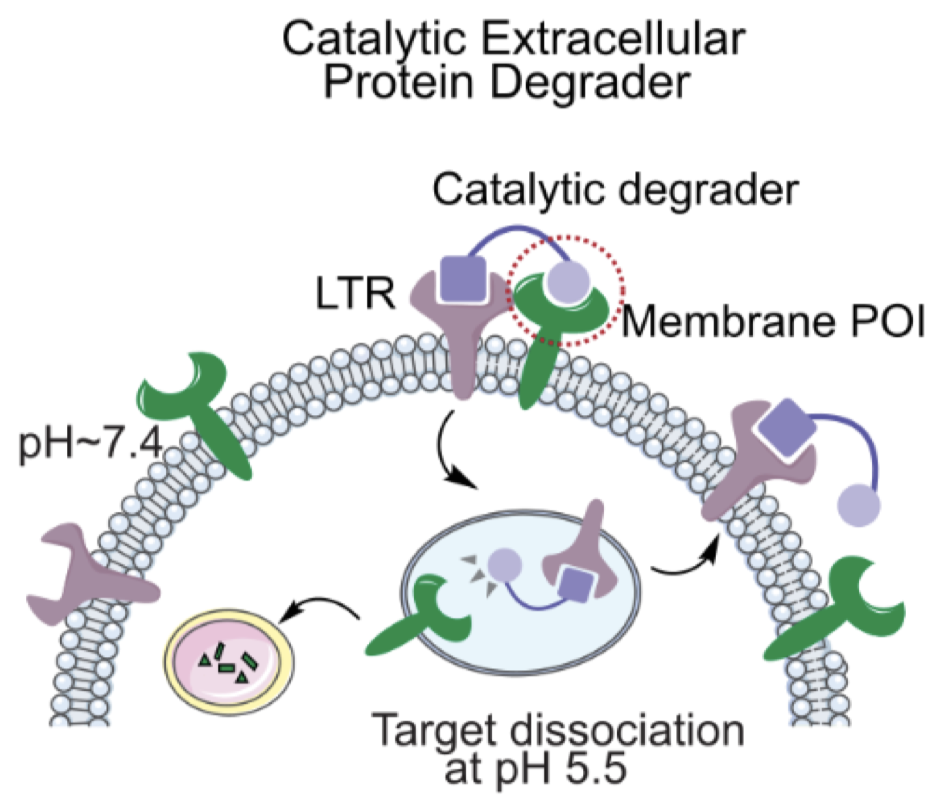
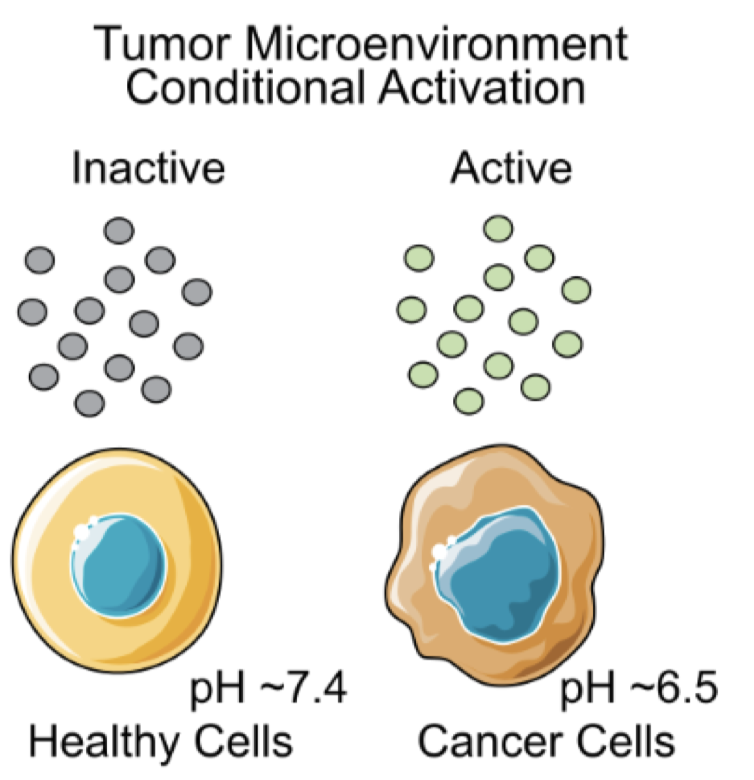
抗体回收 & 蛋白降解 细胞外,PH~7.4 细胞内,PH~5.5 肿瘤微环境 健康细胞,PH~7.4 癌症细胞,PH~6.5
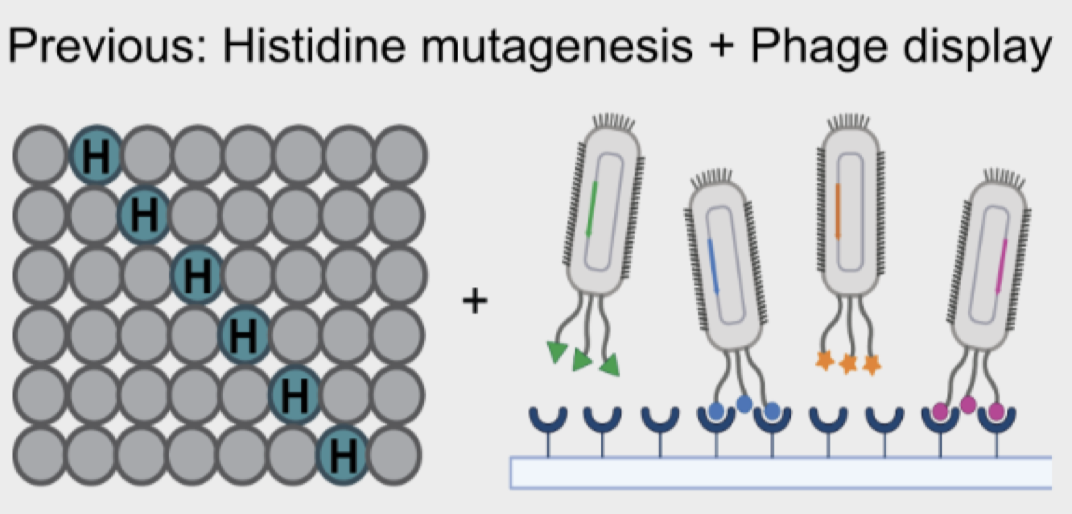
传统方法针对pH敏感性的binder设计,有以下两种方法:
组氨酸扫描 噬菌体展示
本文作者利用蛋白质从头设计方法,去设计pH敏感性的Binder。此Binder的设计目标为:酸性PH条件下解离,中性PH条件下结合。
组氨酸(HIS)是唯一在生理PH下侧链pKa值(~6.5)的氨基酸。它有以下特点:
中性PH条件下,HIS不带电,可作为氢键供体和受体。 酸性PH条件下,组氨酸带正电,只能作为氢键供体。
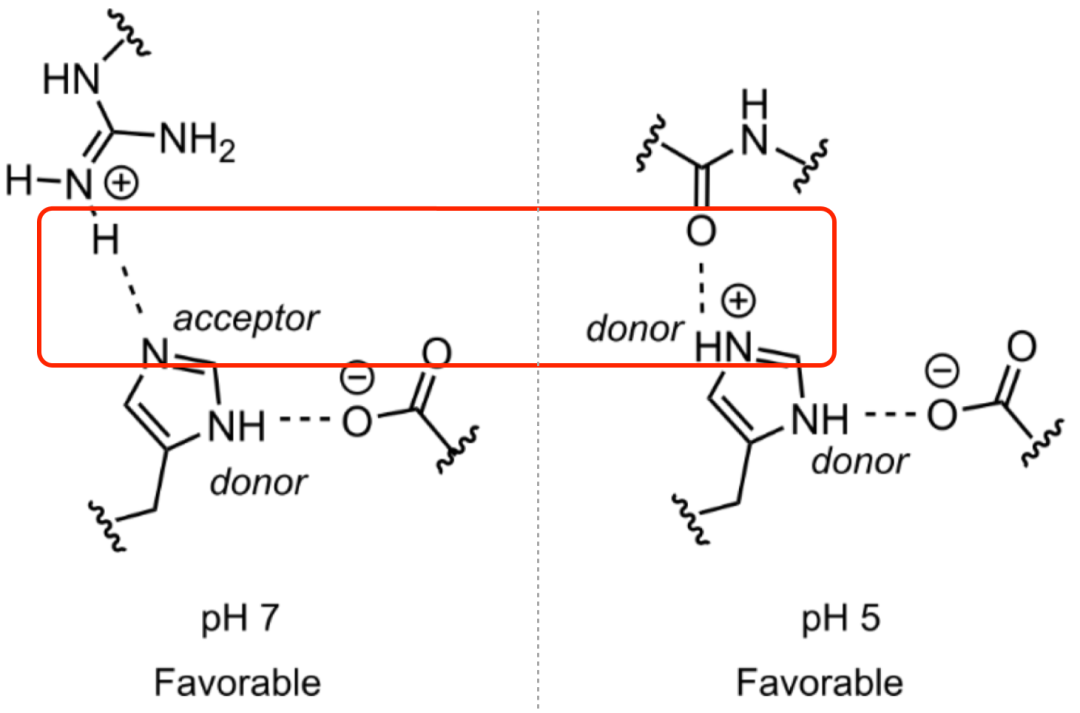
结合组氨酸(H)的这一大特点,作者提出了以下两种计算策略:
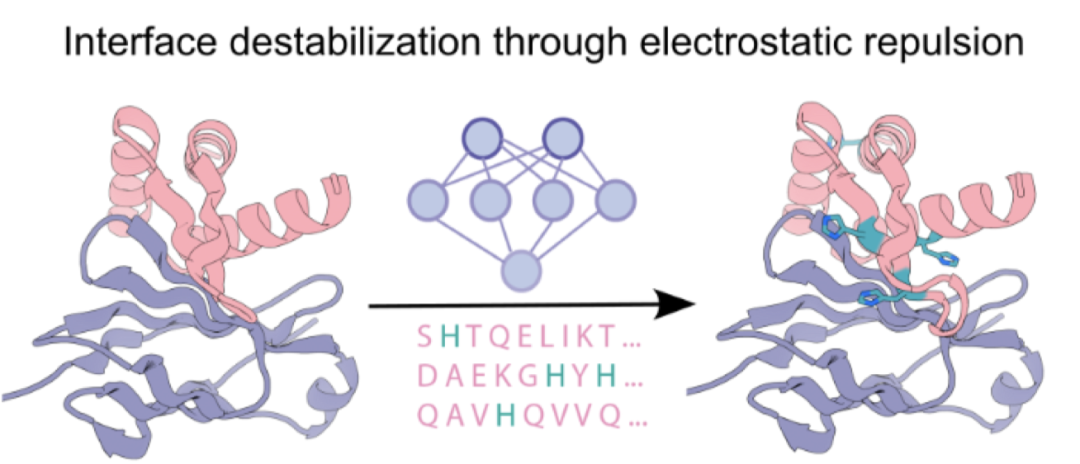
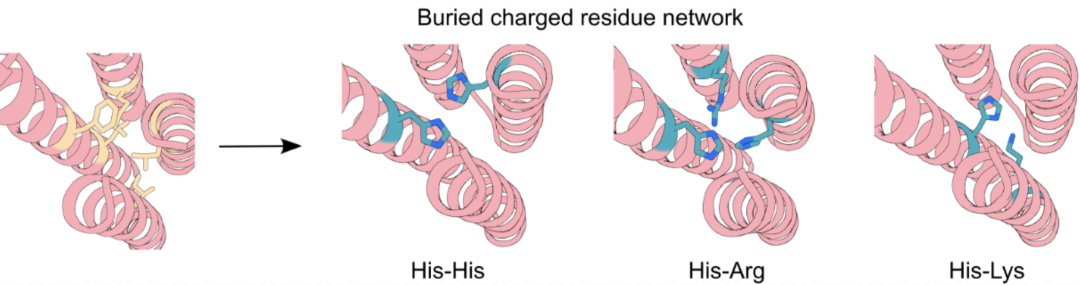
界面destabilization策略:在结合界面引入组氨酸,利用其质子化引发静电排斥和氢键消失。 单体destabilization策略:在binder核心区引入埋藏的电荷网络,利用静电斥力破坏其折叠稳定性。
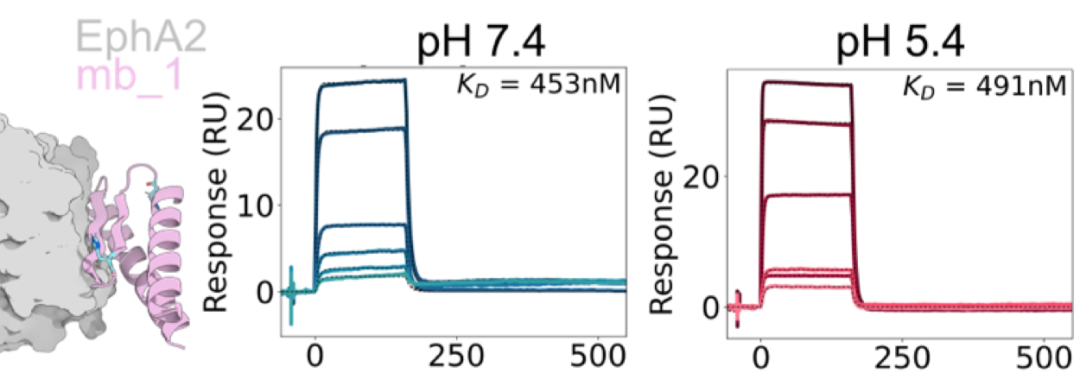
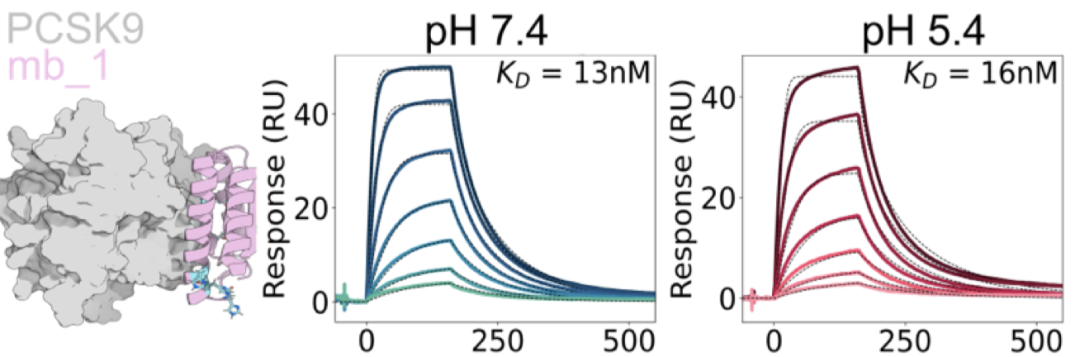
针对EphA2、PCSK9的设计Binder,采用RFdiffusion、HIS-biased ProteinMPNN模型,提高组氨酸HIS的比例。结果表明随机增加组氨酸数量,并不能增加PH敏感性(下图)。
结合上面的经验,作者优化了蛋白设计流程如下:
骨架:针对原有Binder采用Partial RFdiffusion生成大量骨架 序列:HIS-biased ProteinMPNN优化界面并引入组氨酸 过滤:Rosetta评估组氨酸在酸性和中性PH下的氢键模式(供体/受体)、以及氢键埋藏深度,构建了一个PH分数用于筛选 酵母展示筛选:通过酵母展示筛选的12000个设计。结果成功筛选到4个pH敏感性的Binder(下图)。
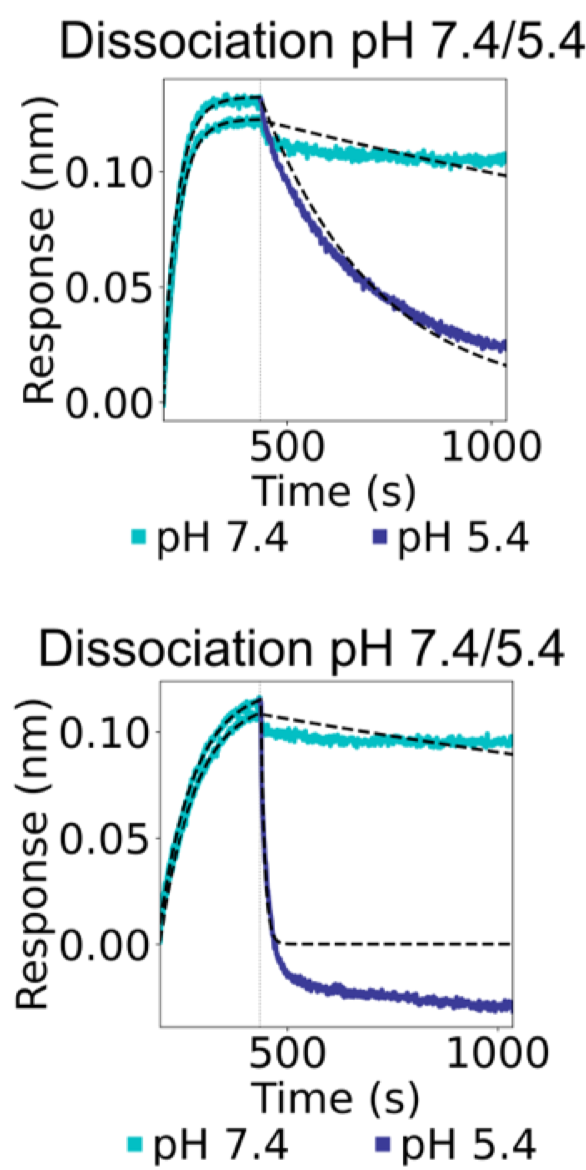
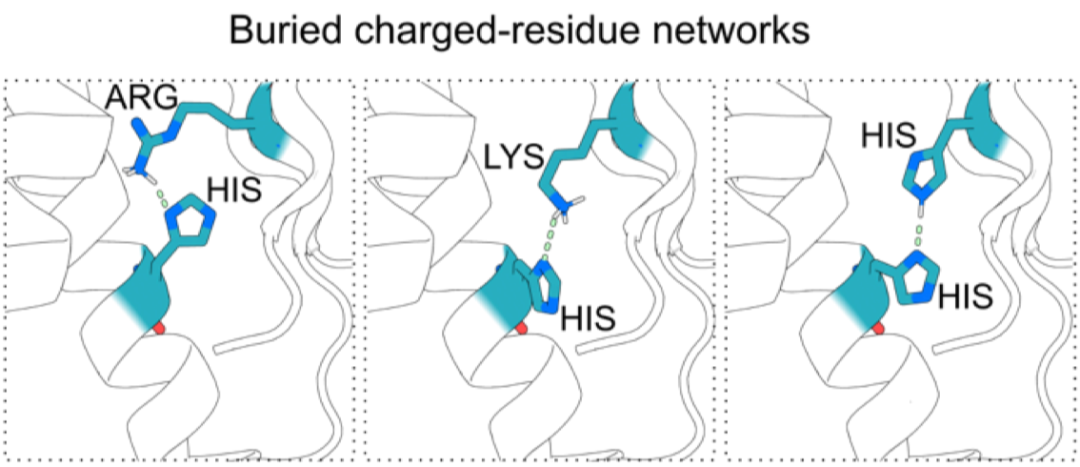
分析:分析这4个成功的Binder,团队发现了一个共同特征:Binder上的His组氨酸残基,都非常靠近靶蛋白(EphA2)上的正电荷残基(如:精氨酸Arg)。 pH=7.4时,组氨酸(H)不带电,与Arg和平共处; pH=5.4时,His组氨酸质子化带正电,与同样带正电的Arg产生强烈的静电排斥,导致结合界面失稳,Binder解离。
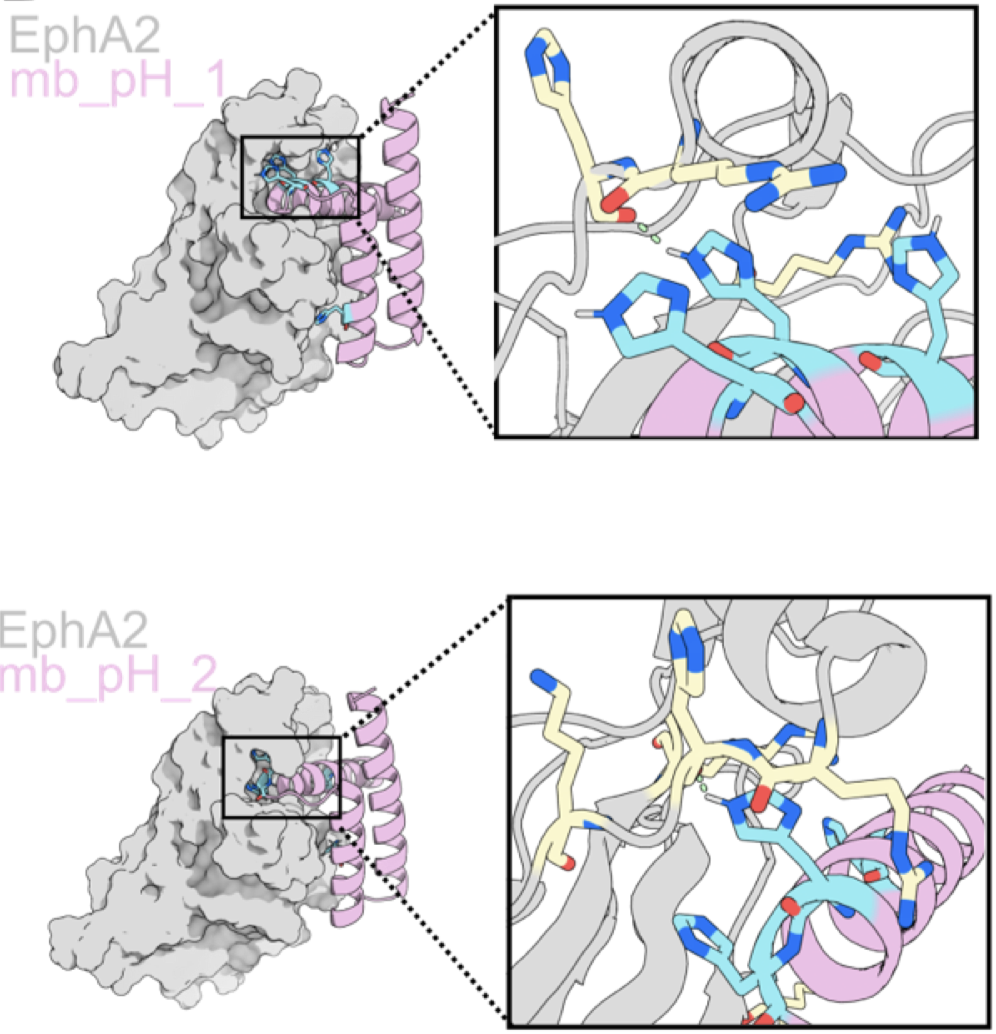
最终策略和上面的流程差不多(下图),如下:
Partial RFdiffusion HIS-biased MPNN AlphaFold2 ddg_elec ≥ 0, 酸性中性PH下的静电能量项差值 且至少有一个HIS作为氢键受体和正电荷残基形成氢键。
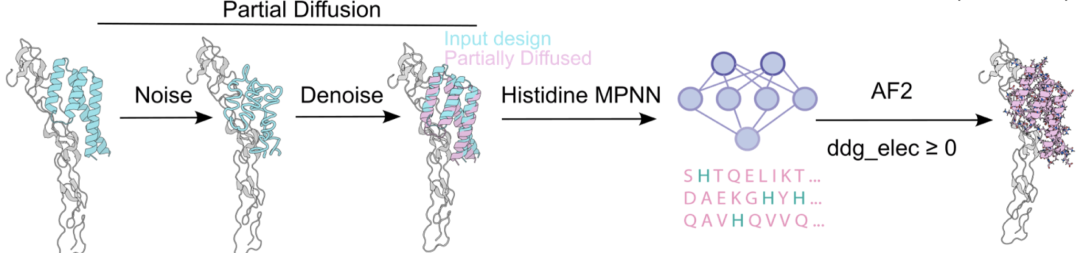
结果显示这一优化策略取得了明显进步,在测试的43个TNFR2的Binder中,有6个表现出pH敏感性,最佳的一个在酸性条件下结合力下降了122倍(下图)。
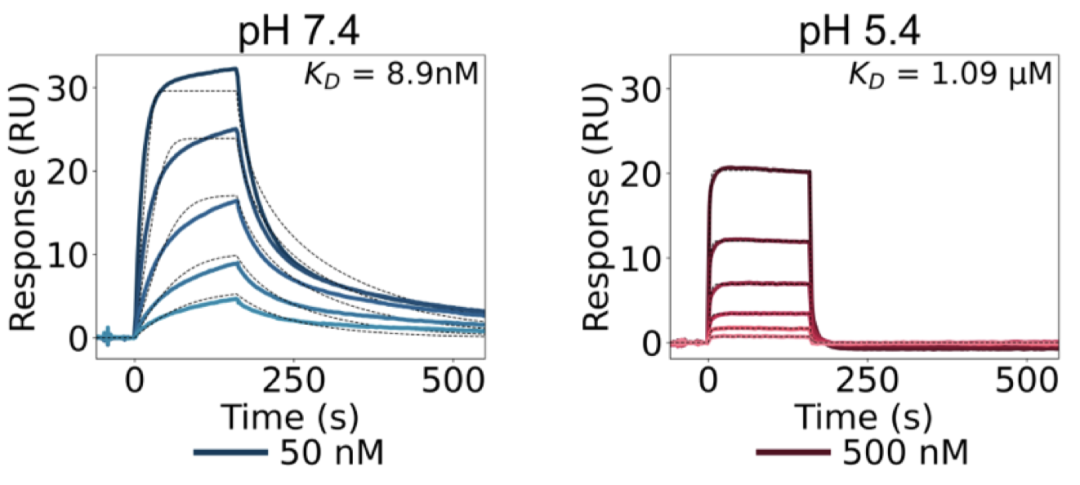
界面destabilization策略虽然成功,但存在一些局限:它依赖于靶蛋白的结合界面上有正电荷残基。于是作者提出了一个互补的单体destabilization策略:在binder的核心区域引入组氨酸His,和正电荷残基(Lys,Arg,His)组成电荷网络,这样就会:
中性条件下His不带电,通过氢键网络维持Binder的稳定折叠, 而在酸性条件下,His带正电和其他正电荷残基产生静电排斥导致Binder自身结构不稳定,从而与靶蛋白亲和力下降导致解离。
PyRosetta脚本在Binder核心区域搜素并植入His形成正电荷网络 ProteinMPNN重新设计周围残基序列 Alphafold2预测结构 过滤确保结构稳定(PAE/RMSD低),且氢键能量良好(<0.5kcal/mol)
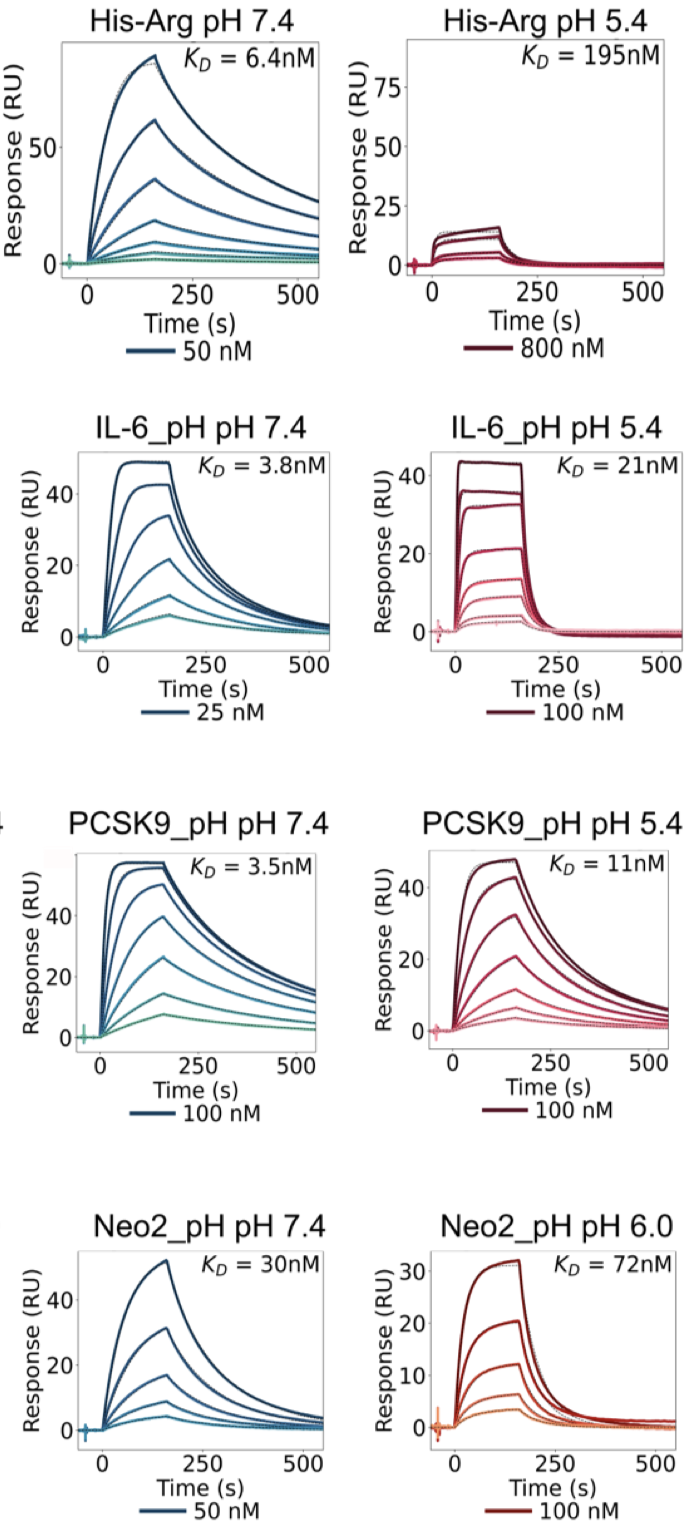
作者团队使用这一策略成功获得了针对TNFα(79倍差异)、IL-6(4倍差异)、PCSK9(3.5倍差异)和Neo2(2.4倍差异)的pH敏感性Binder(下图) 。
文章除了以上的理论研究之外,还进行了下游应用的验证。
LYTACs(溶酶体靶向嵌合体)是一种双功能蛋白,一端结合细胞表面的溶酶体转运受体(LTR),另一端结合靶蛋白。它能将靶蛋白拉到内源性LTR,通过LTR的内吞途径,将其一同送入溶酶体降解。
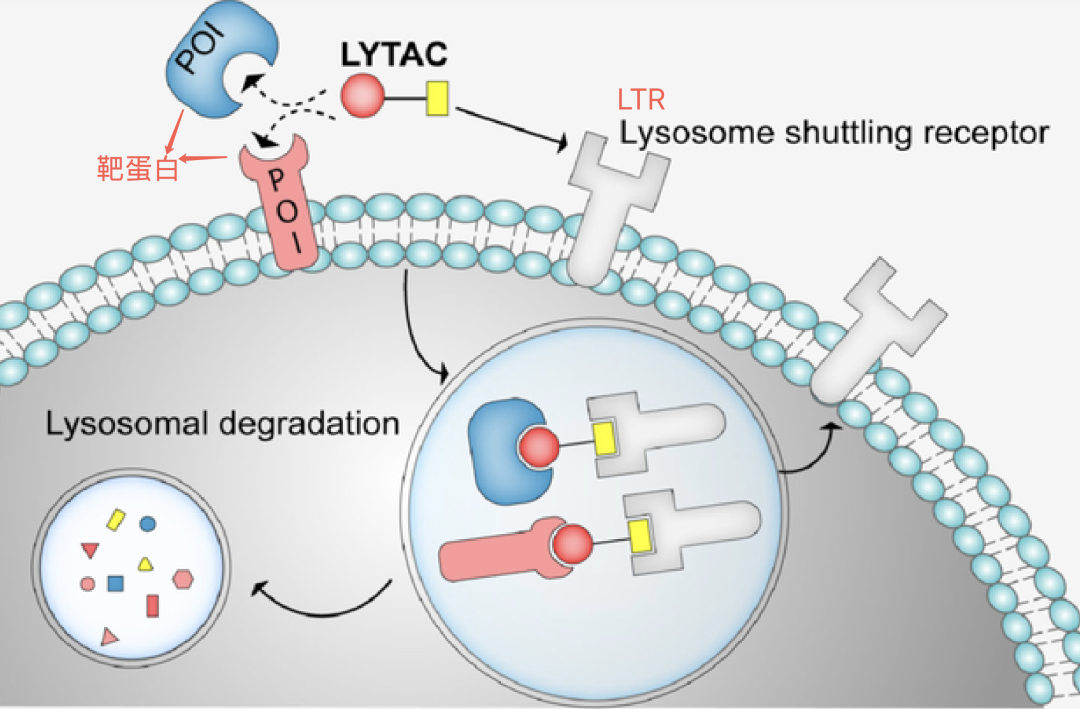
LYTAC存在一个问题:它与靶蛋白结合太牢固,在溶酶体中无法与靶蛋白解离。最终导致LYTAC与靶蛋白一起被降解(见上图)。这意味着一个LYTAC分子只能降解一个靶蛋白分子,效率低下。
作者利用以上方法,设计pH敏感性的Binder,构建出pH敏感性LYTAC(pH_LYTAC):
LTR端:使用一个pH不敏感的Binder(IRigd1),确保在酸性环境中也能牢牢抓住LTR 。 靶蛋白端:使用新设计的pH敏感Binder(如pH_EphA2_mb)。 在细胞外,pH_LYTAC同时结合LTR和靶蛋白。 在细胞内:pH_LYTAC的LTR端保持结合;靶蛋白端松手,释放靶蛋白任其降解。
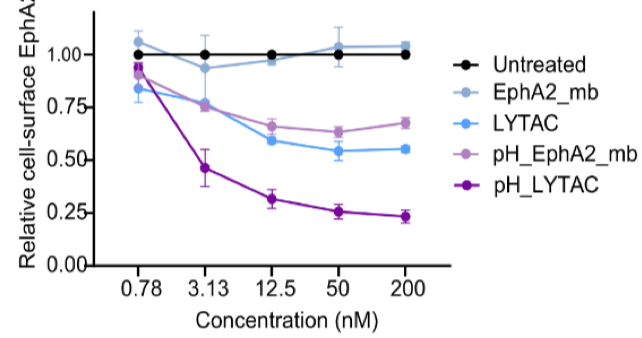
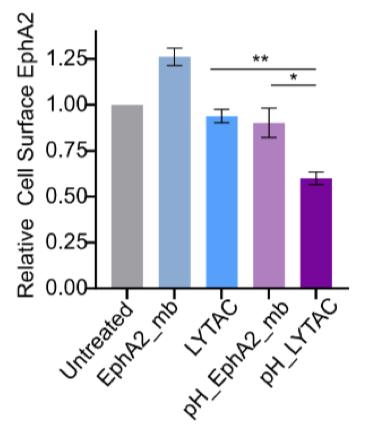
HCT116细胞用不同浓度的设计蛋白处理24小时,通过流式细胞术测量细胞表面EphA2的MFI变化。曲线显示,pH敏感LYTACs在低浓度下即可引发显著降解,EC50值降低,表明其高效性和催化特性,而非pH敏感版本需要更高浓度,这支持了pH设计在降低治疗剂量方面的潜力(下图)。
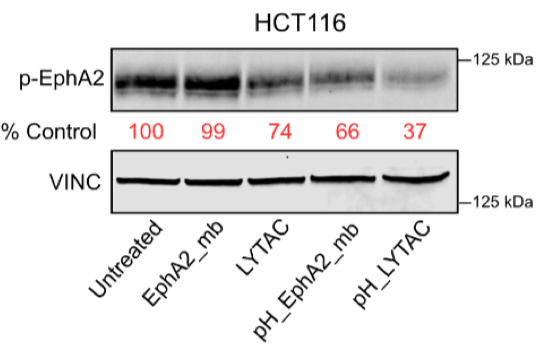
通过Western blot分析了磷酸化EphA2(p-EphA2, Ser897)的水平,这是一种与癌症进展相关的活化形式。在HCT116细胞中,pH敏感LYTACs处理24小时后,p-EphA2信号显著减弱,而总EphA2也相应减少,表明降解不仅清除蛋白,还抑制了其致癌活性。这一结果突出了pH敏感降解剂在靶向疾病相关信号通路中的治疗价值。
这项工作为设计pH敏感性Binder提供了思路,其核心是将氢键网络和静电相互作用力结合起来,指导组氨酸的精确植入。
界面destabilization策略,适用于靶蛋白界面有阳离子残基的情况 。 单体destabilization策略,适用于需要保留原始结合界面,且Binder自身核心区足够大的情况。 通过将pH敏感性Binder引入,作者成功构建了催化型降解剂,极大地提升了LYTACs的治疗潜力。
反向设计:利用相似原理,可以反向设计在酸性pH下结合更紧的Binder(例如,让His质子化后形成新的盐桥),用于TME靶向或抗体半衰期延长。 pKa调控:未来可通过设计His周围的残基,更精确地调节pKa值,使其精准匹配TME的pH 6.5,从而最大化肿瘤选择性和治疗窗口 。 应用:pH敏感性binder为蛋白质治疗、诊断和合成生物学工具提供了强大的条件控制开关。
这是一篇出色和完整的工作,总的来说,这篇文章的novelty是将pH敏感性Binder的设计从经验筛选推进到理性计算的阶段。作者提供了两种清晰、互补的计算策略,并进行了下游应用实验证明其价值。但是小编还是要说一些自己认为的这篇文章的 "不足之处":
理论上单体destabilization应该比界面destabilization更通用,但仔细分析文章数据显示其成功率和敏感性远低于策略一的界面去稳,Neo2的成功率为 2/48 ,TNFα为 3/7。文章没有深入探讨这两个策略设计结果差异这一问题。
界面destabilization能达到122倍的亲和力变化 ,而策略二的效果要弱得多:尤其IL-6仅为6倍 ,PCSK9仅为3.5倍 。在临床上,3.5倍的亲和力差异是否足够构成一个pH敏感性的开关?
本文的设计依赖于组氨酸在~pH 6.5左右的天然pKa。这在区分pH 7.4(血液)和pH 5.5(内体)时是有效的。但是在针对TME时候,我们可能需要一个在pH6.8激活的开关,而不是pH在5.5。如果作者能够重新设计序列精确调控组氨酸的pKa,那这篇工作应该是达到真到的随心所欲设计pH敏感性Binder了。
Ahn, Green, et al. "Computational design of pH-sensitive binders." bioRxiv (2025): 2025-09. 代码:暂未开源
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢