类器官是由干细胞衍生的三维结构,能够重现相应组织的关键结构与功能特征。与传统的二维细胞系相比,人类类器官提供了更接近人体生理状态的实验模型。它们能够捕捉人类组织的复杂性和异质性,从而有助于研究疾病机制、药物疗效及毒性。若类器官源自患者样本,还可用于预测个体化的药物反应,为精准医疗提供支持。
2025年11月12日, Hubrecht研究所、Oncode研究所与罗氏研发中心的研究人员在《Nature Reviews Drug Discovery》期刊上发表了一篇综述文章,题为“Human organoids as 3D in vitro platforms for drug discovery: opportunities and challenges”。
在这篇综述中,研究团队探讨了类器官在药物发现领域的应用价值。概述了类器官的生成与维持的方法学,讨论了其在疾病建模、药物筛选和安全性评估方面的应用,并考虑了监管方面的问题以及其在药物研发更广泛应用所面临的挑战。
背景
在药物发现过程中,体外模型通过提供可控的实验系统来研究细胞对药理作用的反应,发挥着关键作用。传统上,人类细胞系因其相对简单、成本低廉以及在实验室中易于获取,被视为药物发现的主要工具。然而,这些细胞系多来源于肿瘤,并被适应性培养在二维塑料表面,因而缺乏真实组织的空间结构,也不具备器官内部多种功能性细胞类型。这些局限促使研究者发展更具生理相关性的三维培养系统,如类器官,以更精准地模拟体内微环境。与动物实验相比,类器官成本更低,能实现高通量筛选(HTS),同时避免了物种差异和动物实验相关的伦理问题。
近年来,多能干细胞(PS细胞)来源类器官的标准化制备流程得到了快速推进。这些方案通常持续数周至数月,以小聚团形式的诱导多能干细胞(iPS细胞)为起点,通过优化营养供给并模拟发育过程中依次出现的信号环境,引导PS细胞向特定组织方向分化(图1a)。由PS细胞构建的类器官已能模拟多种组织,包括大脑、视网膜、肺、肾、肝和肠道。与此类似,组织干细胞(TSCs)的扩增与分化依赖特定的生长因子和细胞外基质成分,以生成目标组织类型的类器官(图1b)。与基于PS细胞的方法不同,TSC类器官直接来源于活组织(如活检样本),无需经历体外的谱系指定过程。
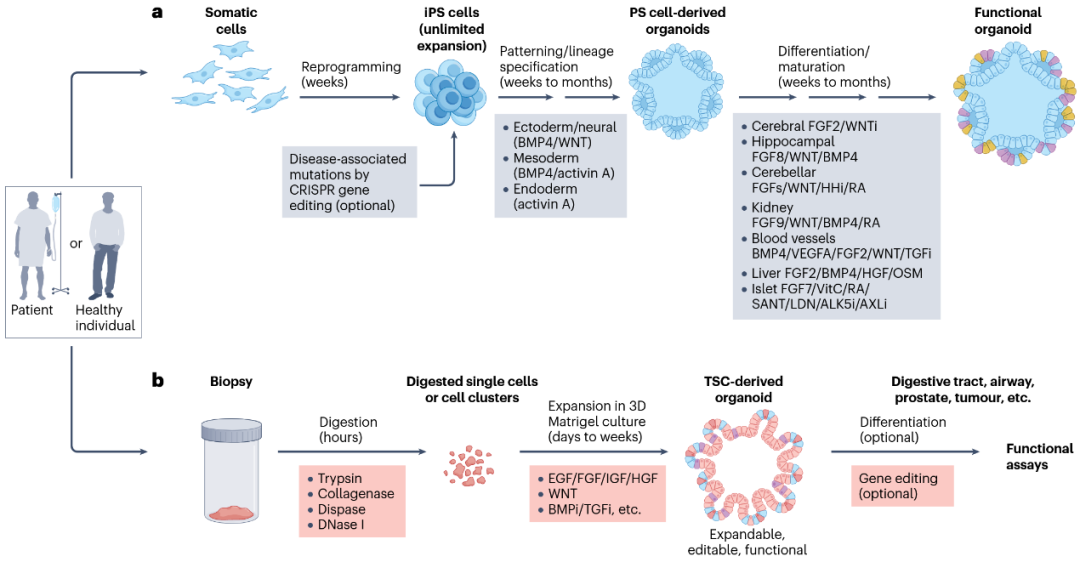
图1 来源于多能干细胞与组织干细胞的人类类器官
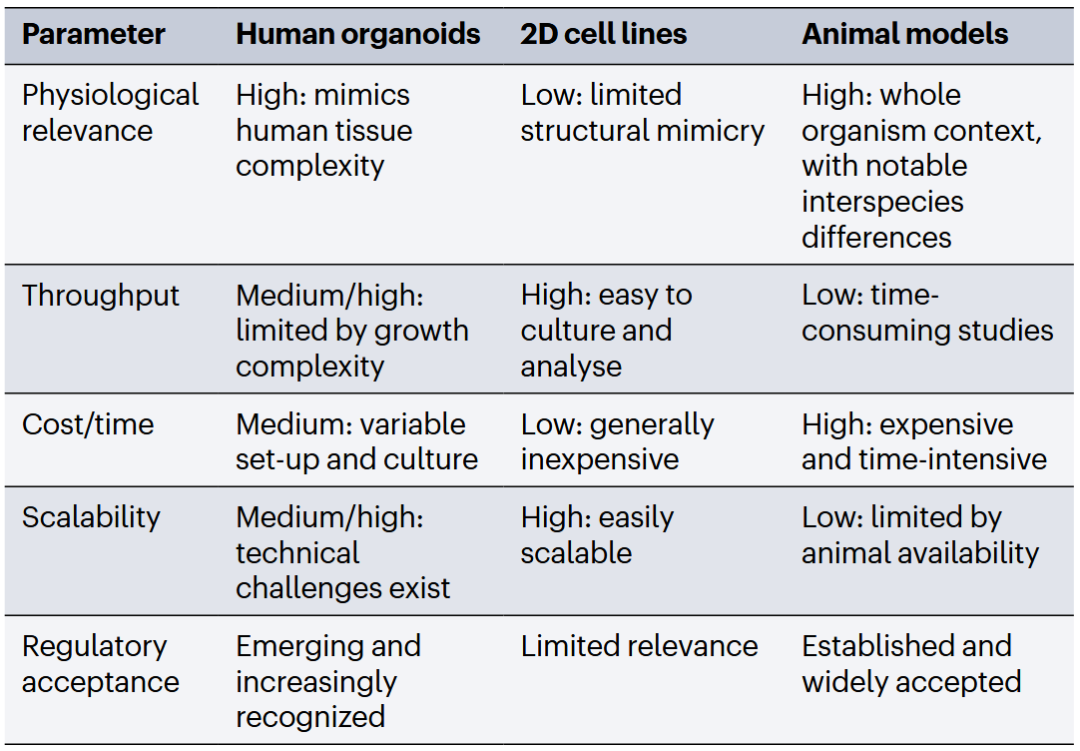
在过去十年中,类器官相关的研究数量迅速增长。人类类器官提供体外实验模型,可补充传统的二维人类细胞系和动物模型(表1)。该综述系统总结了类器官的建立与维持方法,并重点阐述了其在疾病建模、治疗筛选、药物药理研究及毒性评估中的应用。同时,作者特别讨论了类器官在精准医学领域的潜力,当类器官由患者来源细胞构建时,可用于个体化药物反应预测。文章最后还分析了当前在监管体系中的相关考量,以及类器官平台在成为药物开发成熟工具之前仍需解决的关键挑战。
表1 人类类器官与传统临床前模型的比较
疾病建模
类器官已被应用于多种疾病领域,包括遗传性疾病、癌症和传染病(图2)。它们能够重现真实器官(病理)生理特征,如大脑、肾脏、肝脏、肺和肠道。与永生化细胞系相比,类器官具备更复杂的三维组织结构,呈现出明确的区域特异性与正确的细胞极性,并包含多种成熟细胞谱系,能够支持多种功能性实验。此外,类器官表达关键受体以及必要的细胞内成分,可实现病原体的有效入侵,并支持其完整生命周期的复制。这些独特属性(图上方)使类器官成为研究遗传疾病、感染性疾病及多类型肿瘤等多种病理过程的重要工具。进一步地,通过引入免疫细胞等微环境组分,类器官还可用于模拟并探索炎症性疾病,为理解疾病机制及开发潜在治疗策略提供新的实验平台。图下方展示了已成功通过类器官建模的疾病示例。
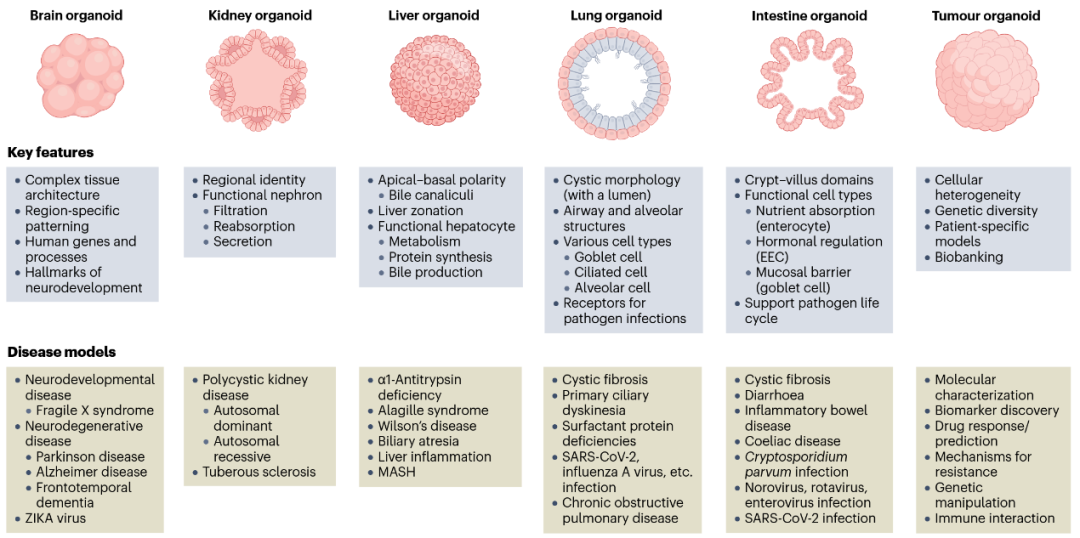
图2 疾病建模中不同类型的类器官
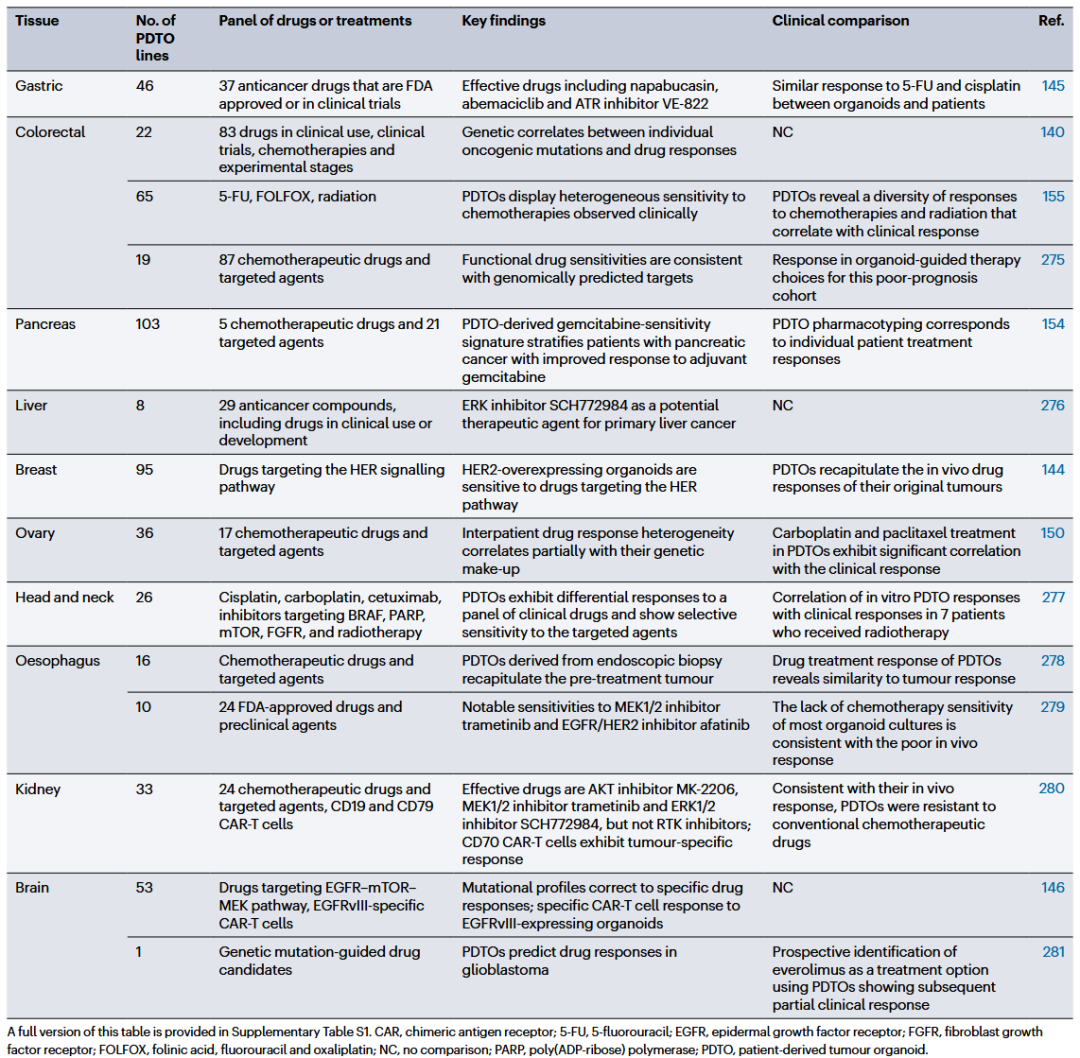
以癌症研究为例,许多肿瘤类型(如胰腺癌、肝癌和乳腺癌)并不会在动物中自发形成;即便通过引入癌症关键突变进行诱导,肿瘤的发生通常需要较长时间,且所得模型仍难以完全再现人类肿瘤的复杂性与异质性,包括其遗传多样性和免疫微环境特征。过去十年间,患者来源肿瘤类器官(PDTOs)的发展显著扩展了临床前癌症模型的可用资源库。PDTOs几乎可由所有主要实体瘤构建,起始材料可来自活检或切除样本。这些培养物具备良好的可扩增性,能够高度再现原发肿瘤的组织学、基因组和转录组特征,并可稳定移植至小鼠体内进行进一步的功能研究。PDTOs及与之配对的健康组织来源类器官已针对多种肿瘤类型建立并系统性地储存在生物库中(表2)。这些PDTOs既反映了肿瘤间异质性,也反映了肿瘤内异质性,使其可用于研究肿瘤演化和进展、测试治疗反应的差异性、理解耐药机制及发现新的治疗靶点。
表2 药物筛选与评估的代表性PDTOs生物库
药物安全性的转化应用
尽管大多数研究集中于类器官在药物疗效和疾病建模方面的应用,但其在制药行业中的使用正在扩展,用于评估药物化合物对多个器官的安全性(表3)。
表3 类器官在药物安全性评估中的应用
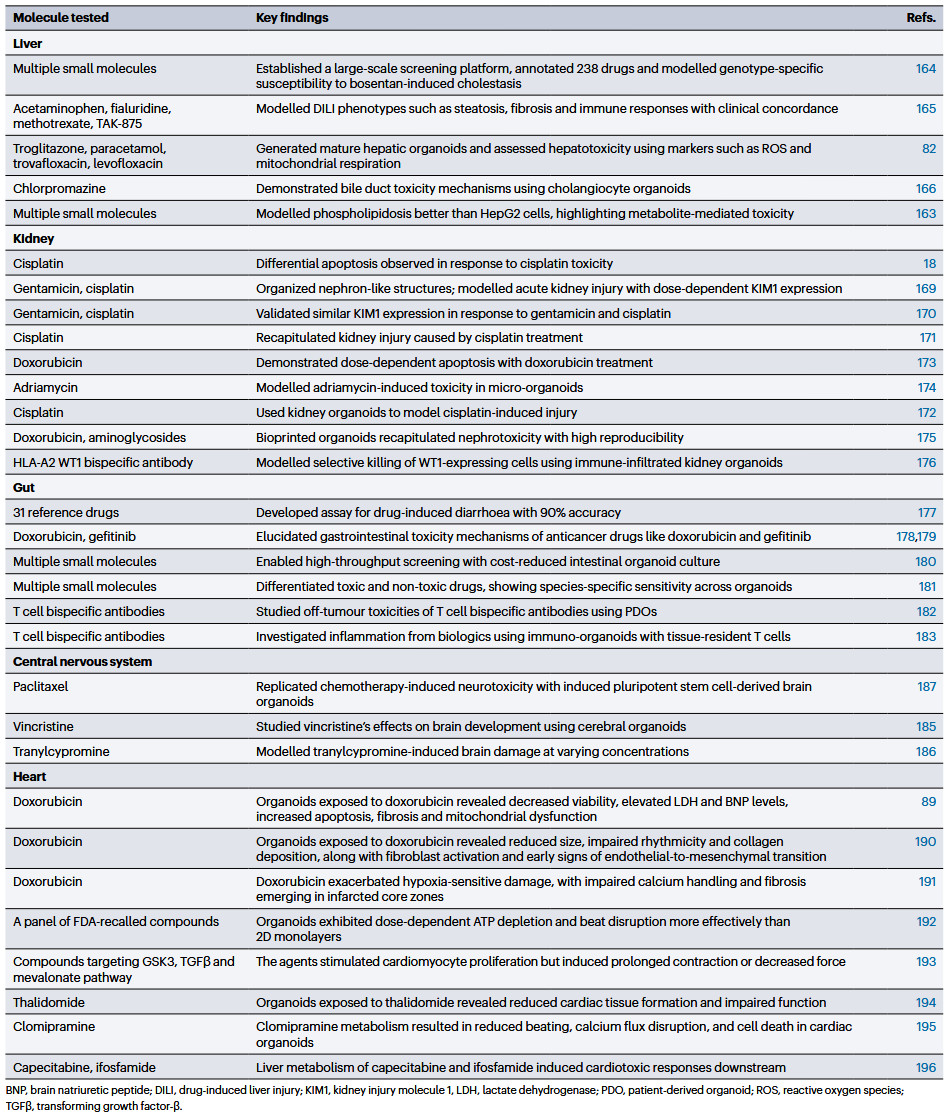
肝脏在药物代谢中起核心作用,而药物性肝损伤是导致药物开发失败、市场撤回和批准后使用受限的主要原因。功能成熟的PS细胞来源人肝类器官(HLOs)能够再现已知药物的肝毒性,例如troglitazone(一种因肝毒性被撤市的抗糖尿病药)、对乙酰氨基酚(paracetamol,也称acetaminophen,一种广泛使用的止痛药)以及抗生素trevafloxacin和levofloxacin,在临床相关浓度下的敏感性高于二维肝细胞。同样地,TSC来源HLOs在模拟药物诱导的磷脂沉积症(phospholipidosis,一种严重的不良反应)方面优于传统的肝癌细胞HepG2,显示其评估代谢物介导肝毒性的能力。
药物诱导的神经毒性是候选药物开发终止的主要原因,已报道中枢神经系统(CNS)不良反应导致7–34%的早期和晚期药物研发项目被终止。类器官为揭示传统方法难以检测的毒性机制提供了强有力的模型。再者,利用类器官模型对小分子和大分子药物的胃肠道毒性进行更精准的预测,可显著改善临床前风险–收益评估,并减少药物开发过程中因毒性而被淘汰的比例。此外,尽管已开发和应用多种预测性临床前检测方法,心脏毒性仍然是药物开发失败及上市后撤药的主要原因之一。由干细胞衍生心肌细胞及支持性细胞组成的人类心脏类器官应能够重现心脏组织结构、收缩功能及电生理特征的关键方面,从而为预测药物对心脏反应提供替代方法。
传统类器官预测现有药物安全性的能力正在探索中,而新一代生物工程类器官平台已显示出进一步改善药物安全性检测的潜力(图3b)。这些模型可整合血管和免疫成分,使研究者能够考察药物对组织微环境和系统性反应的影响;或通过内置生物传感器实时检测ATP/ADP比值来评估药物诱导的肾毒性。近期,生物工程化二维类器官(如迷你结肠芯片和迷你肠芯片)进一步扩展了药物安全性评估能力,通过维持类器官分化和顶底极性,同时利用流体流动便于腔道访问(图3a)。这些将类器官生物学与生物工程方法相结合的先进平台,为应对具有复杂作用机制的药物所带来的转化安全性挑战提供了新方案。
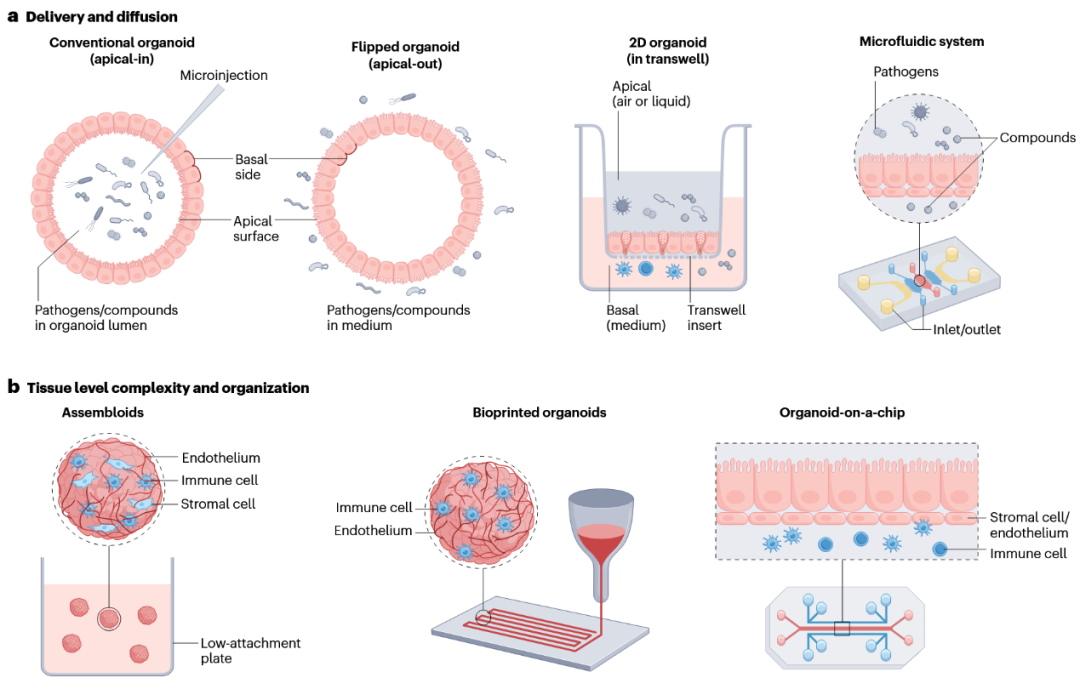
图3 疾病建模与药物安全性评估中的先进类器官系统
基于类器官的药物吸收与代谢检测
肝脏是药物代谢的主要器官。当前最先进的体外模型存在局限性,包括无法完全复制肝脏代谢及转运表型(原代人肝细胞在培养中迅速衰退)、细胞与培养基比例不理想影响代谢与转运过程的可测性,以及胆汁分泌能力有限。肝细胞系的药物代谢酶和转运蛋白表达水平不佳,限制了对人体药代动力学的预测能力。为解决这一问题,研究人员开发了一种来源于TSC的肝脏类器官系统,该系统表达广泛的I相药物代谢酶、Ⅱ相酶及药物转运蛋白。该系统与毫微流体芯片集成,已用于研究咪达唑仑(midazolam)的代谢与生物利用度,以及在多器官平台(结合肠道和肾脏类器官)中考察香豆素(coumarin)和二甲双胍(metformin)的排泄。
早期概念验证研究显示,肠道类器官系统有助于更好地理解和预测肠道药物吸收及代谢。TSC衍生的肠道及肝脏类器官可通过地塞米松(dexamethasone)、β-萘黄酮(β-naphthoflavone)及构成型雄烷受体激动剂TCPOBOP成功诱导CYP酶活性,从而进行药物代谢研究。事实上,小鼠来源的肠隐窝类器官已被用于研究肠道药物代谢酶(DME),显示前药CPT-11可转化为其毒性代谢物SN-38。
类器官在药物吸收、分布、代谢及排泄(统称ADME)研究中的应用仍有限。关键挑战包括肝脏与肾脏类器官分化的相对不成熟。此外,尽管存在可转化性问题,在动物体内进行小规模药代动力学研究相对简单,其便利性常超过基于类器官平台预测的潜在优势。
当前挑战的潜在解决方案
其中一个障碍在于,尽管类器官比细胞系复杂得多,但它们仍属于简化模型,缺乏真实组织的关键元素。另一个主要障碍是类器官培养的可变性,导致可重复性难以保证。传统的类器官药物筛选方法包括将类器官嵌入基质中,然后播种到多孔板中,并在上方加入培养基。自动化机器人和液体处理系统可以简化这一流程(图4a)。生物工程微流控设备能够快速生成大量重复类器官,这些类器官嵌入在少量细胞外基质(ECM)中,可支持类器官极性和存活。这些设备可将类器官播种到多孔板、多孔/微阵列或微柱芯片中(图4a–d),允许对类器官的形状、大小和细胞数量进行精确控制,从而大大提高均一性和可重复性(图4b)。微孔阵列(图4c)已被用于分析肺癌类器官,可在一周内预测药物反应;而在384微柱板中培养的3D神经干细胞(图4d)可实现大规模化学库的神经毒性筛选。
早期的自动化发展进一步提升了类器官与微流控HTS平台的整合(图4e)。一个例子是Mimetas的organoplate,它能够实现自动换液、精确控制环境条件,甚至进行药物筛选,几乎无需人工干预。该平台已被用于肝类器官的肝毒性检测和肺类器官的呼吸系统疾病建模,展示了自动化在药物筛选和疾病建模中的潜力。
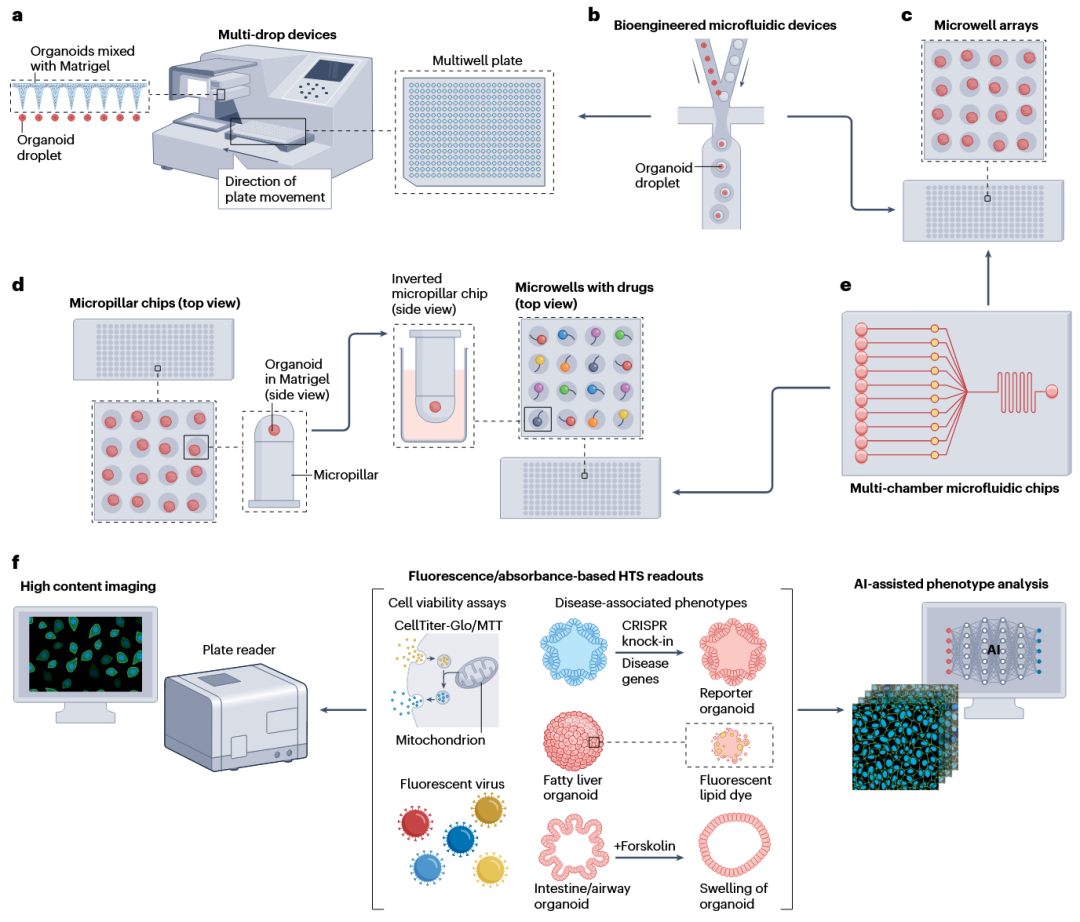
图4 自动化高通量药物筛选策略
总结
类器官在药物开发中的应用,为前临床研究提供了更精准、更贴近患者的模型,实现了转型式的飞跃。如前所述,类器官平台能够重现人类组织的复杂性,比传统的二维细胞培养和动物模型提供更生理相关的环境。然而,尽管该领域已取得重要进展,仍存在挑战。类器官培养的可扩展性和可重复性,尤其是在高通量筛选中的应用,仍需进一步优化。这将要求持续开发和验证标准化、自动化的类器官平台,并建立清晰的监管框架以促进产业应用。此外,为增强类器官对人类治疗反应的预测能力,尤其是在癌症、神经退行性疾病以及慢性炎症和代谢疾病等复杂疾病中,还需在血管化、免疫系统整合和多器官建模方面进行创新,并结合先进的分析技术,如单细胞组学、高速图像采集及AI支持的数据分析。随着技术成熟,预计类器官平台将成为药物发现流程的核心组成部分,桥接基础科学与临床结果之间的差距。类器官有望彻底改变我们对疾病的理解与治疗,其在药物开发中的未来潜力巨大。
参考链接:
https://doi.org/10.1038/s41573-025-01317-y
--------- End ---------
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢