DRUGONE
精准预测抗体–抗原复合物结构对于抗体治疗开发至关重要,但传统抗体发现仍依赖动物免疫或库筛选,效率低且难以针对特定表位。研究人员构建 tFold System,整合抗体结构预测(tFold-Ab)、抗体–抗原复合物预测(tFold-Ag)、结构引导的虚拟筛选,以及表位特异性抗体的 de novo 设计。借助该系统,研究人员成功设计出针对 4 种治疗相关抗原(Flu A、PD-1、PD-L1、SARS-CoV-2 RBD)的单克隆抗体,并通过表面等离子共振实验验证,其亲和力达到纳摩尔至皮摩尔水平,且具有精确的表位特异性。tFold System 为快速、高通量、面向特定表位的抗体发现提供了计算–实验一体化解决方案。

抗体在适应性免疫中扮演核心角色,是最重要的治疗蛋白之一。然而,当前抗体开发依赖动物免疫或噬菌体展示筛选,流程耗时、昂贵且对特定表位的控制有限。
近年来虽然出现了基于结构预测、能量优化、反向折叠等计算设计方法,但针对抗体的 de novo 设计仍进展缓慢,主要受限于:
抗体结构数据稀缺——可用于训练的抗体结构远少于一般蛋白。
抗原–抗体界面复杂——大量由无序环区构成,预测难度高。
抗体–抗原复合物预测不够可靠——现有模型对抗体体系表现不佳。
缺乏可针对任意表位进行设计的系统化流程。
因此,构建一个 端到端、可高通量运行、能够直接输出表位特异性抗体的计算系统,成为抗体设计领域的重要目标。
方法
tFold System 由生成模型与结构筛选模块组成:
输入抗原序列、目标表位及抗体框架序列;
生成器随机采样大量抗体序列,并由 tFold-Ab 与 tFold-Ag 预测其结构;
通过 ipLDDT、预测复合物置信度等指标对候选抗体进行结构引导的虚拟筛选;
低置信度区域通过掩蔽—重建循环优化;
输出能够稳定结合目标表位的抗体序列与结构。
最终,候选序列进入噬菌体展示筛选和 SPR 实验验证。
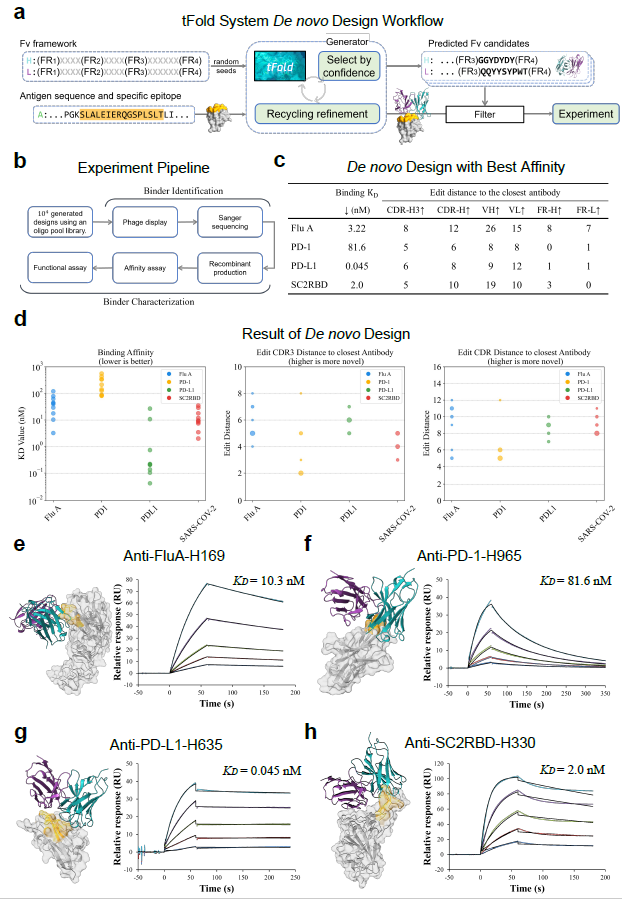
图1:tFold System 在 de novo 抗体设计中的整体流程与实验性能概览
结果
tFold System 成功设计出高亲和力抗体
研究人员针对 Flu A、PD-1、PD-L1 和 SARS-CoV-2 RBD 生成并筛选大量抗体候选。实验结果显示:
设计抗体的亲和力达到 纳摩尔至皮摩尔水平;
PD-L1 抗体中出现亚 100 pM 的高亲和力分子;
Flu A 与 SARS-CoV-2 RBD 的最佳抗体亲和力分别为 3.22 nM 与 2.0 nM。
SPR 动力学曲线展示其快速结合与慢速解离特性;结构模型确认抗体可稳定结合指定表位。
此外,序列比对表明设计的 CDR 区域具有高度新颖性,避免了对已知抗体的简单模仿。
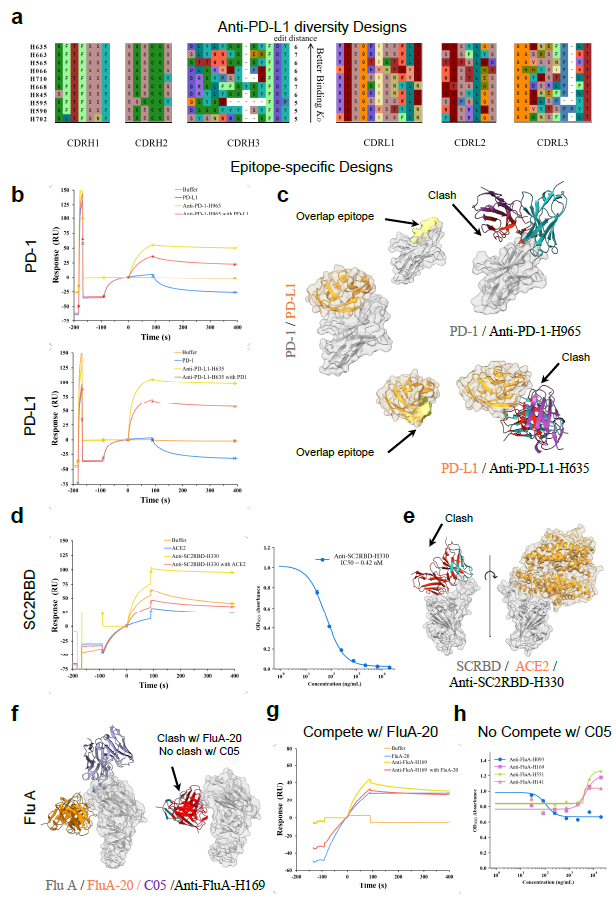
图2:tFold System 展示了按预期靶向抗原表位的多样化抗体设计能力。
设计的抗体具备明确的表位特异性
研究人员通过竞争结合实验验证抗体是否真正靶向指定表位:
PD-1/PD-L1 系列:设计的多株抗体能够有效阻断 PD-1–PD-L1 结合,符合免疫检查点抑制的功能需求。
SARS-CoV-2 RBD:部分抗体可强效阻断 ACE2 结合,其中最高亲和力抗体的中和能力 IC50 为 0.42 nM。
Flu A:设计抗体与已知广谱抗体 FluA-20 在表位上呈竞争关系,说明成功捕获其关键抗原决定簇。
结构叠合进一步显示设计抗体的结合面位置与靶向表位高度一致。
tFold-Ab:快速精准的抗体结构预测
tFold-Ab 由预训练蛋白语言模型(ESM-PPI)、Evoformer-Single、结构模块和循环模块组成,可在数秒内预测抗体的原子级三维结构。
其优势包括:
不依赖 MSA,速度比传统方法快数十至上千倍;
在 FR 与 CDR 区域均取得更高预测精度,尤其在最难的 CDR-H3 上表现最佳;
在抗体与纳米抗体数据集上均达到领先性能。
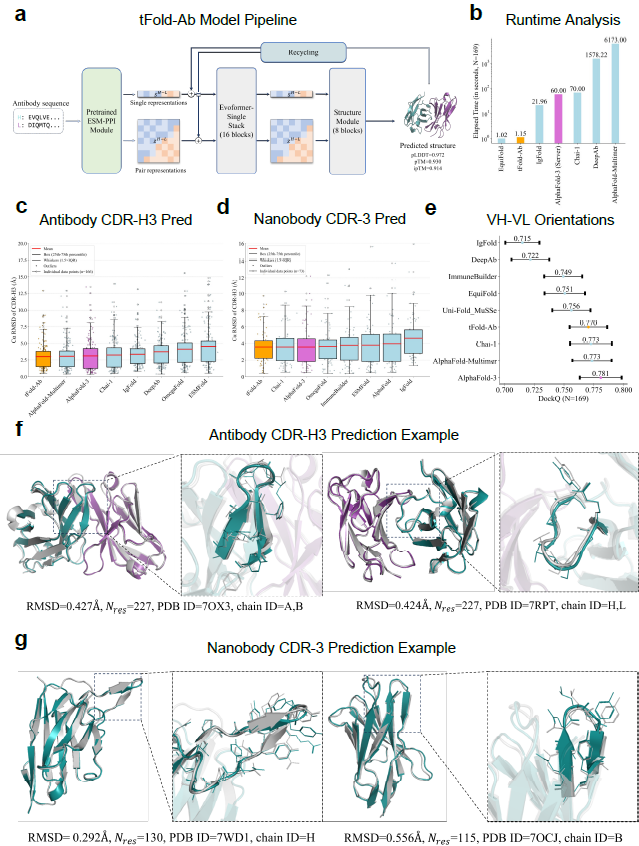
图3:tFold-Ab 的整体框架与性能评估
tFold-Ag:快速预测抗体–抗原复合物
tFold-Ag 由抗体特征单元、抗原特征单元和柔性对接单元组成,可预测复合物结构并提供可用于筛选的置信度分数。
特点包括:
速度比 MSA 方法快数十倍;
在 DockQ、成功率等指标上优于大多数现有工具;
能整合表位/互补位点约束,提高界面预测准确性;
置信度指标与真实结构精确度高度相关,可用于快速筛选。
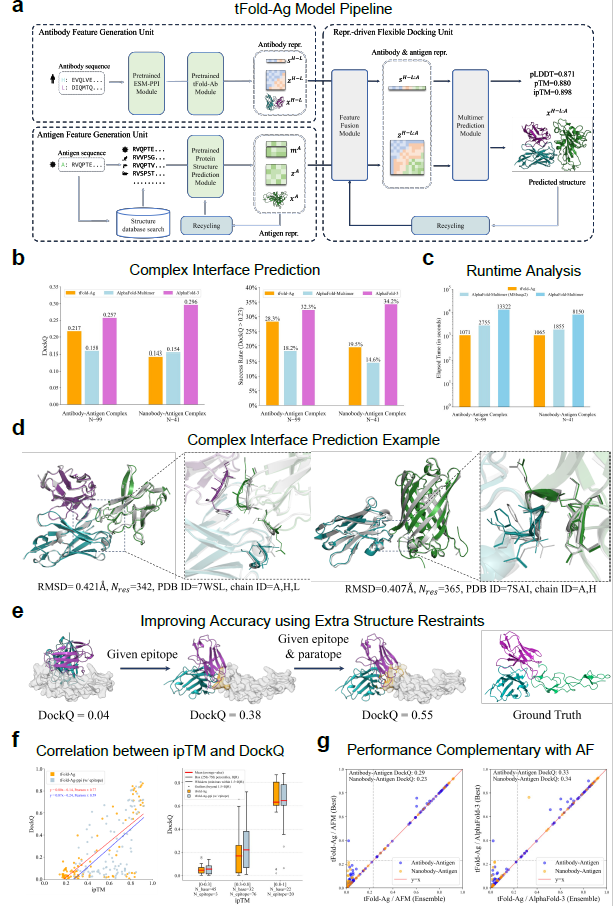
图4:tFold-Ag 的全面分析与性能评估
结构引导的虚拟筛选能有效识别真实结合抗体
研究人员利用 tFold-Ag 的预测置信度在两类任务中验证筛选能力:
自然抗体库筛选:AUC 可达 0.7–0.76,前 1% 排名中富集率显著高于随机。
de novo 抗体的抗原特异性选择:在 PD-1、PD-L1 和 Flu A 任务中能区分正确结合的抗体。
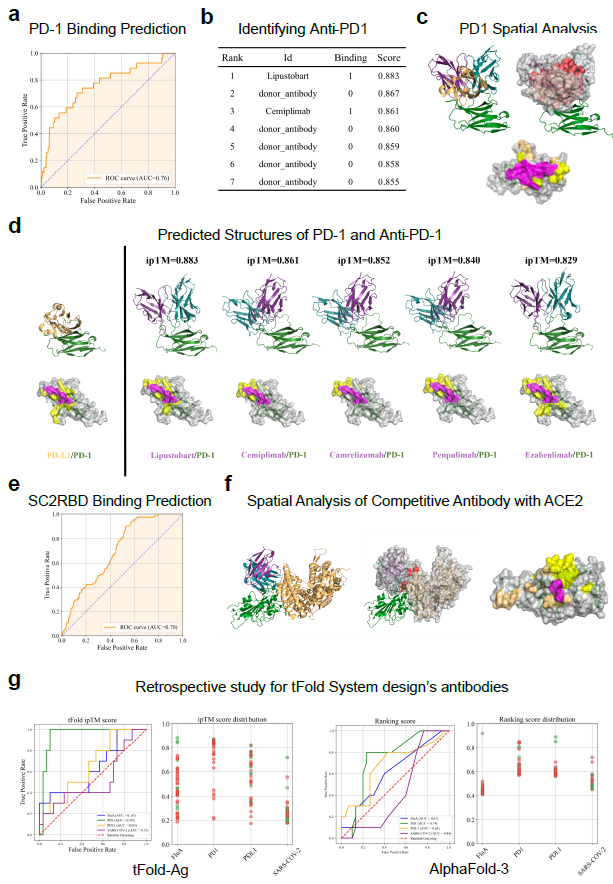
图5:利用 tFold-Ag 进行结合抗体的结构引导型虚拟筛选
tFold System 可联合进行结构预测与序列恢复,实现真正的端到端设计
通过多任务训练,tFold-Ag 既能预测复合物结构,也能恢复被掩蔽的 CDR 序列,实现结构–序列联合优化。
在多个测试集上,tFold-Ag 在 CDR-H3 恢复 上达到与需要先验表位信息的方法相当或更高的水平;
逐位生成策略可避免“YYY” 过度频繁 motif 造成的设计多样性损失;
输出的抗体序列结构保持合理构象,并具备实验验证价值。
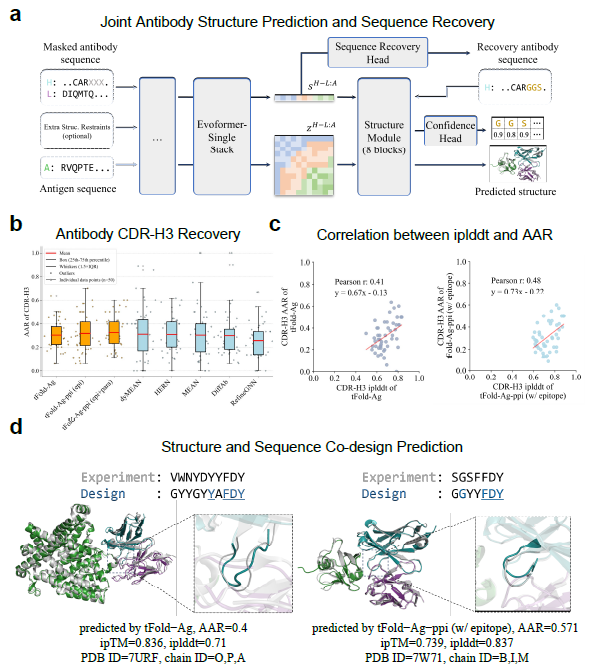
图6:基于 tFold-Ag 的抗体结构预测与序列联合恢复
讨论
tFold System 通过计算生成 + 结构筛选 + 实验验证的组合,实现了表位特异性抗体的全新设计,并在多类关键靶点上获得可进入药物开发阶段的候选分子。
系统的优势包括:
能直接针对指定表位进行设计(传统免疫无法做到);
可与噬菌体展示等高通量实验管线无缝衔接;
在抗体亲和力、靶点多样性、功能验证方面均取得成功。
仍需提升的方面包括:
对“真结合–不结合”区分度有限;
对序列微变与抗原突变的敏感度不足;
对纳米抗体与复杂抗原体系预测尚不够稳健;
对训练数据中未出现过的特殊表位预测存在困难。
未来可将 AlphaFold-3 等更先进结构工具纳入筛选流程,以提高虚拟筛选准确度和设计成功率。
整理 | DrugOne团队
参考资料
Wu, F., Zhao, Y., Wu, J. et al. De novo design of epitope-specific antibodies via a structure-driven computational workflow. Nat Commun (2025).
https://doi.org/10.1038/s41467-025-67361-9

内容为【DrugOne】公众号原创|转载请注明来源
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢