2025 年 11 月发表在《Nature Communications》一篇药物诱导性肝损伤(DILI)预测的研究论文,其核心是构建了目前规模最大的毒性转录组学资源与高效预测框架,为药物研发中的肝毒性风险评估提供了新方案。
研究思路
构建 了大规模数据库DILImap :
这是研究打造的目前规模最大的 DILI 专用 RNA-seq 数据库,涵盖 300 种化合物,包含 DILI 阳性、阴性、特异体质型等不同类型,且每种化合物设置了多个浓度梯度。数据生成过程中,在保障细胞活性和 RNA 质量的前提下,还通过 LDH/ATP 活力检测、IC10 剂量筛选等操作,同时结合 DILIrank 与 LiverTox 进行分类,并构建了含 51 个化合物的独立盲测数据集,为后续模型训练奠定了坚实的数据基础。
开发了高性能AI模型 ToxPredictor :
该框架是机器学习驱动的毒性基因组学工具。其先解析药物暴露 24 小时后人源初级肝细胞的 RNA-seq 转录组变化,提取差异基因与通路的激活模式,再结合临床 DILI 标签,用随机森林集成模型(30 个随机森林模型组合)开展训练。最终能输出剂量分辨的 DILI 概率,还可结合临床血药峰浓度建立安全边界,实现对药物肝毒性风险的分类和相关机制解析。
关键研究结果:预测性能领先:盲测验证中,ToxPredictor 框架展现出优异性能,达到 88% 的灵敏度和 100% 的特异性,远超 3D 肝模型、传统细胞毒性检测等 20 多种行业标准临床前安全模型。它还成功提前识别出 Evobrutinib、TAK-875 等多款在临床三期因肝毒性失败的候选药物,这些风险此前均未被动物实验发现。
DILImap 数据库的核心构建方法为 RNA-seq,那么是否有操作更便捷,通量更高的技术能更快速产生药物扰动转录组数据呢?
昕瑞再生开发的 DRUG-seq 2技术,凭借 “仅需 1000 个细胞 / 样本、免 RNA 提取、成本显著更低” 的核心优势,实现了少量细胞的高通量转录组测序突破;对于 AI 大模型构建所需的大规模数据节点积累而言,DRUG-seq2 无疑是效率更高、成本更优的最佳技术利器。
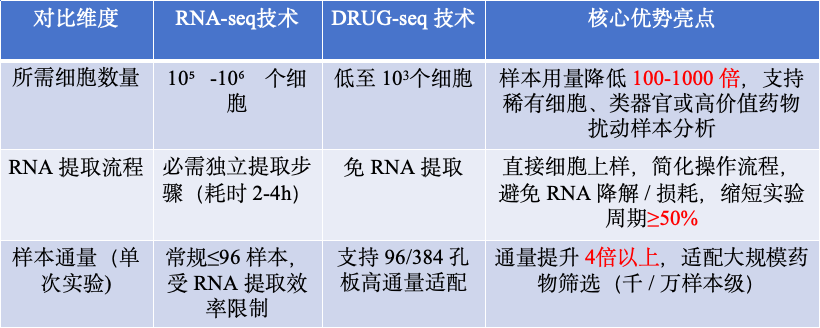
DRUG-seq2相比RNA-seq技术核心亮点
昕瑞再生还建立了自动化建库设备,可以实现每周上万样本速度高效生成扰动转录组数据,满足“数十万分子扰动+百万转录组响应”的高数据需求。
自主搭建的高通量自动化文库构建系统
关于昕瑞再生
南京昕瑞再生医药科技有限公司成立于 2019 年,先后获中科创星、红杉资本两轮融资,依托北京大学分子医学南京转化研究院软硬件支持。公司创始人是北京大学赵扬老师,承载创始团队在干细胞、再生医学及小分子创新药领域 20 余年经验,搭建了世界领先的细胞表型药筛平台—— 整合细胞疾病模型、表型组学定量、AI 技术,聚焦 “细胞疾病 / 衰老表型逆转” 研发新药。
公司拥有自主知识产权的DRUG-seq2、PHDs-seq 高通量测序技术,已在早期药物发现、细胞毒性测试和AI模型建立等场景见效,既服务自研项目,也为科研领域提供高质量技术解决方案。
联系方式:
南京昕瑞再生医药科技有限公司
www.xremed.com
南京市江北新区磐固路16号
18936040318

内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢