
生命科学
Life science


激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2−)乳腺癌是乳腺癌中最常见的亚型,约占全部病例的三分之二。对于晚期患者,内分泌治疗联合CDK4/6抑制剂已成为一线标准方案,中位无进展生存期可达2至2.5年。
然而,一旦患者对CDK4/6抑制剂产生耐药,后续治疗选择有限,标准护理尚未明确,现有治疗策略的中位无进展生存期通常不超过6个月,临床需求远未得到满足。


▲长按图片识别二维码阅读原文
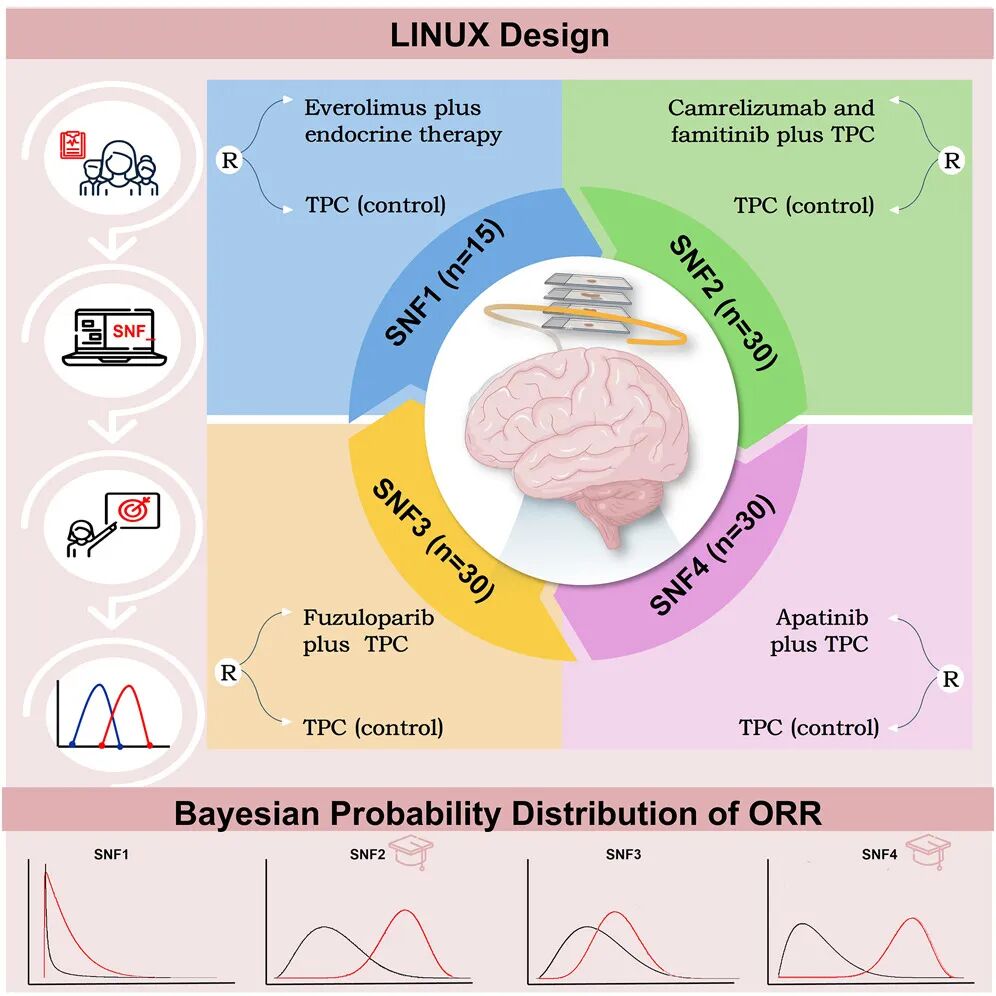
研究团队此前通过整合基因组学、蛋白质组学和代谢组学等多维度数据,利用相似网络融合这一先进的计算生物学方法,成功地将这一看似均一的疾病解构为四个具有鲜明生物学特征的亚型:SNF1(经典型管腔亚型),其特征是对内分泌治疗相对敏感但增殖活性较低;SNF2(免疫亚型),展现出显著的免疫细胞浸润和激活状态,提示其可能对免疫治疗有应答;SNF3(增殖亚型),伴有DNA损伤修复缺陷和高染色体不稳定性,理论上对PARP抑制剂敏感;以及SNF4(RTK驱动亚型),其受体酪氨酸激酶信号通路异常活跃,是抗血管生成靶向治疗的潜在用武之地。然而,多组学检测的高成本和操作复杂性限制了其临床普及。为此,研究者巧妙地开发了一套基于卷积神经网络的深度学习模型,该模型能够仅从医院常规采集的H&E染色病理切片中,提取出与这些深层分子特征相关联的形态学信息,从而实现对SNF亚型的精准、快速且低成本的预测,其交叉验证的曲线下面积高达0.87至0.78,为大规模临床应用的可行性提供了坚实的技术保障。
从2022年12月到2024年5月,六家研究中心共筛查了132例患者,最终105例符合严格标准的患者被随机分配至基于分型的精准治疗组或医生选择治疗组。这些患者群体代表了临床上面临最大治疗困难的人群,她们全部接受过CDK4/6抑制剂联合内分泌治疗且发生进展,超过半数曾接受过针对转移灶的化疗,部分患者还曾进行靶向治疗、免疫治疗乃至抗体药物偶联物,中位治疗线数达到2线,且绝大多数患者存在两个及以上器官的转移,近八成伴有内脏转移,尤其是肝转移比例高达62%,这些都预示着其肿瘤负荷重、预后差。截至2025年5月的数据分析时,中位随访时间已达18.3个月,绝大多数患者因疾病进展而停止了研究治疗,这为疗效评估提供了相对成熟的数据。
试验的核心发现体现在其主要终点——客观缓解率上,其结果清晰地描绘出不同亚型对特定精准治疗策略的迥异反应。在SNF1亚型中,采用mTOR抑制剂依维莫司联合内分泌治疗的精准方案,其客观缓解率仅为10%,而对照组医生选择治疗更是低至0%。更关键的是,贝叶斯监测模型计算出其客观缓解率低于20%的后验概率高达85.7%,触发了预设的无效终止边界,这使得该亚型的精准治疗组提前停止了患者招募,后续该亚型患者均被分配至对照组,这一决策本身就体现了适应性试验设计在避免资源浪费和患者暴露于无效治疗方面的伦理与科学价值。与之形成鲜明对比的是SNF2和SNF4亚型。SNF2患者接受的是卡瑞利珠单抗(PD-1抑制剂)、法米替尼(VEGFR抑制剂)联合医生选择治疗的三药方案,其客观缓解率飙升至65%,远超对照组的30%,且其疗效优于对照组的后验概率达到86.7%。SNF4亚型的结果更为惊人,使用阿帕替尼(VEGFR2抑制剂)联合医生选择治疗的方案,取得了70%的客观缓解率,是对照组(20%)的三倍多,后验概率高达97.6%,以压倒性优势达到了预设的成功标准。然而,SNF3亚型的结果则令人深思,其采用的氟唑帕利(PARP抑制剂)联合医生选择治疗,客观缓解率为40%,虽数值上高于对照组的30%,但后验概率显示其优势并不显著(39.8%),未能达到成功标准。从整体人群看,精准治疗组51%的客观缓解率显著优于对照组的23%,凸显了分型指导策略的宏观价值,但亚型间的巨大差异更警示我们“一刀切”治疗模式的局限性。
研究的次要终点结果进一步巩固和细化了主要终点的结论。在临床获益率方面,SNF2和SNF4亚型的精准治疗组分别达到了80%和75%,均显著优于各自对照组(40%和30%),这表明治疗带来的疾病控制不仅是深度的,也是持久的。而在SNF1和SNF3亚型中,两组的临床获益率则不相上下。无进展生存期的数据与客观缓解率高度吻合:SNF2亚型中,精准治疗组将中位无进展生存期从4.3个月延长至8.1个月,疾病进展或死亡风险降低了60%;SNF4亚型更是将中位无进展生存期从3.4个月提升至7.0个月,风险降低了66%。这两个亚型的生存曲线分离明显,具有统计学意义。反观SNF1和SNF3亚型,其精准治疗组与对照组的中位无进展生存期则无本质差异。目前总生存期数据尚不成熟,仅有10%的患者发生事件,这需要更长时间的随访来获得最终答案。
在安全性方面,精准治疗策略展现出可控的安全性特征。任何等级的治疗相关不良事件在两组中均普遍发生,值得注意的是,3-4级严重不良事件的发生率在精准治疗组和对照组完全相同,均为37%,这说明在现有治疗框架下,增加针对性的靶向或免疫药物,并未显著提升整体的高级别毒性负担,但其毒副谱系则因治疗方案而异。具体来看,SNF1亚型的毒性主要与依维莫司相关,表现为口腔炎、肝功能异常和贫血;SNF2亚型则突出了免疫检查点抑制剂和抗血管生成药物联合的特点,以免疫性肝炎、肾上腺功能不全为主;SNF3亚型因PARP抑制剂与化疗联用,骨髓抑制成为最主要的剂量限制性毒性;SNF4亚型则典型地体现了阿帕替尼的副作用,即手足综合征、高血压和蛋白尿。两组因不良事件导致的治疗中止率相近,剂量调整比例也完全相同,这表明尽管精准治疗方案引入了新的毒性,但在临床严密管理下是基本可控的。
对55例患者进行的基因组测序揭示了HR+/HER2−乳腺癌后线常见的驱动基因突变,如PIK3CA(51%)、TP53(36%)和ESR1(22%)。进一步的单变量分析发现了一些可能与疗效相关的基因突变,例如在SNF1精准治疗组中,NCOR1突变可能与更短的无进展生存期相关;在SNF2组中,TP53突变反而可能与更长的无进展生存期相关;而在SNF4组中,GATA3突变则提示预后不良。这些发现虽然仅为探索性且需要更大样本验证,但为未来寻找预测性生物标志物指明了方向。组织病理学分析确认了各亚型的预期特征:SNF1组织学分级和Ki67指数较低,SNF2具有较高的肿瘤浸润淋巴细胞水平,SNF4则富含癌症相关成纤维细胞。然而,分析也发现,单独使用肿瘤浸润淋巴细胞或癌症相关成纤维细胞这些单一的形态学指标,并不能有效区分同一亚型内治疗应答者与非应答者,这强调了基于人工智能的多特征整合模型在预测复杂性方面的优越性,以及开发更综合预测工具的必要性。
综上所述,LINUX试验作为一项开创性的随机对照平台研究,首次在HR+/HER2−晚期乳腺癌中验证了基于人工智能分型的精准治疗策略的临床价值。研究成功识别出对免疫联合抗血管治疗敏感的SNF2亚型和对阿帕替尼联合化疗敏感的SNF4亚型,其疗效显著优于传统化疗,且安全性可控。尽管SNF1和SNF3亚型的精准治疗方案未达主要终点,但其结果为进一步优化治疗策略提供了重要线索。该研究不仅展示了人工智能在整合形态学与分子特征方面的强大能力,也为实现真正意义上的“个体化”乳腺癌治疗奠定了坚实基础。

相关文章信息

论文原文刊载于Cell Press细胞出版社
旗下期刊Cancer Cell,
点击“阅读原文”或扫描下方二维码查看论文

▌论文标题:
Precision treatment with artificial intelligence assisted subtyping enhances therapeutic efficacy in HR+/HER2− breast cancer: The LINUXtrial
▌论文网址:
https://www.sciencedirect.com/science/article/abs/pii/S1535610825004969
▌DOI:
https://doi.org/10.1016/j.ccell.2025.11.003

▲长按图片识别二维码阅读原文
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢