DRUGONE
药物组合是肿瘤和感染性疾病治疗中的核心策略,但随着药物数量增加,组合空间呈指数级膨胀,使系统性实验筛选在现实中难以开展。研究人员提出 Combocat,一个将声波液体分配技术与机器学习推断相结合的开源药物组合筛选平台。该平台在保证高剂量分辨率的同时,大幅降低实验成本与操作复杂度,并成功在单一细胞系中筛选了超过 9000 种药物组合,展示了前所未有的筛选规模与效率。

联合用药能够通过协同作用提高疗效、克服耐药性并降低毒性,因此在现代医学中不可或缺。然而,药物组合筛选面临一个根本瓶颈:
一方面,高密度剂量矩阵对于准确识别协同作用至关重要;另一方面,实验资源往往迫使研究人员在“组合数量”和“剂量分辨率”之间做出妥协。
尽管自动化液体处理技术已显著提升实验灵活性,但长期以来缺乏一个将高通量实验设计与组合特异性数据分析紧密整合的完整平台,限制了药物组合筛选的规模化发展。
方法概述
Combocat 是一个端到端的开源平台,涵盖实验设计、数据处理与协同分析三个环节。平台提供两种互补的筛选模式:
高密度模式:在标准化实验流程下,对两个药物的所有剂量组合进行系统测量,获得高保真协同响应图谱;
稀疏模式:仅测量关键剂量点与单药响应,并利用基于机器学习的预测模型推断其余组合响应,从而显著减少实验测量数量。
通过这种“实验 + 预测”的协同设计,Combocat 实现了高精度与高通量之间的平衡。
结果
高密度药物组合筛选的标准化实现
研究人员首先构建了一个统一的高密度筛选流程,在每一对药物之间生成完整且可重复的剂量响应矩阵。该流程在数据质量、归一化和协同量化方面均表现出良好稳定性,为后续建模提供了可靠参考数据。
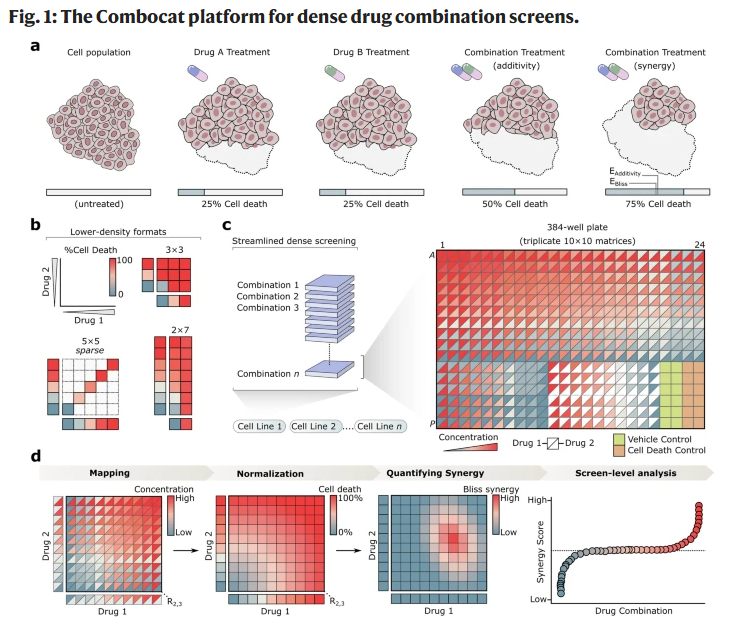
图 1|Combocat 平台的整体架构与高密度筛选流程。
构建大规模参考数据集
利用高密度模式,研究人员生成了一个覆盖多种药物与细胞类型的组合响应数据集,包含数十万条实验测量值。质量控制分析表明,该数据集具有良好的重复性,并能够准确复现已知的经典协同药物组合。
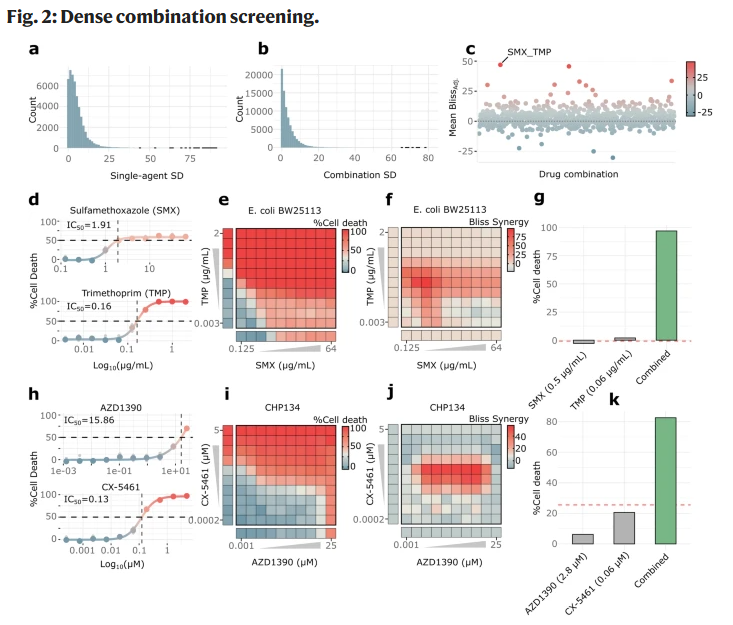
图 2|高密度模式下药物组合响应与协同分布特征。
机器学习辅助的稀疏筛选策略
在此基础上,研究人员训练了一个由多个子模型组成的机器学习推断系统,用于从稀疏测量中重建完整的剂量响应矩阵。结果显示,该模型能够以极高准确性预测未测量的组合响应,从而将实验需求减少约一个数量级。
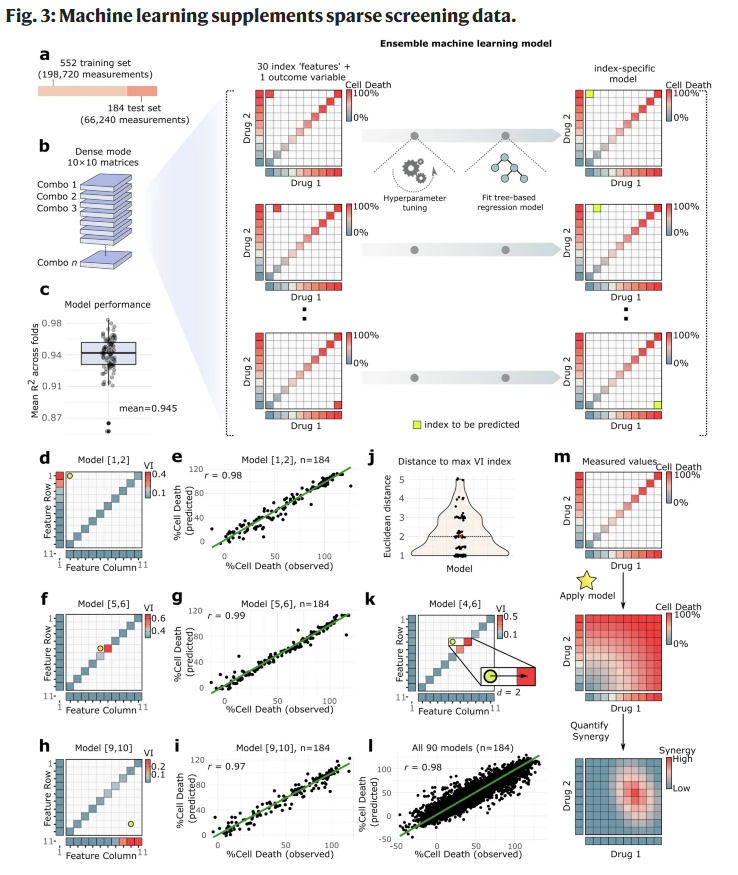
图 3|稀疏筛选中机器学习模型的训练与预测性能。
超大规模药物组合筛选示范
作为概念验证,研究人员在单一肿瘤细胞系中筛选了超过 9000 种药物组合,这是目前在单一体系中报道的最大规模组合筛选之一。筛选结果不仅成功识别出大量潜在协同组合,还在后续验证实验中保持了良好一致性。
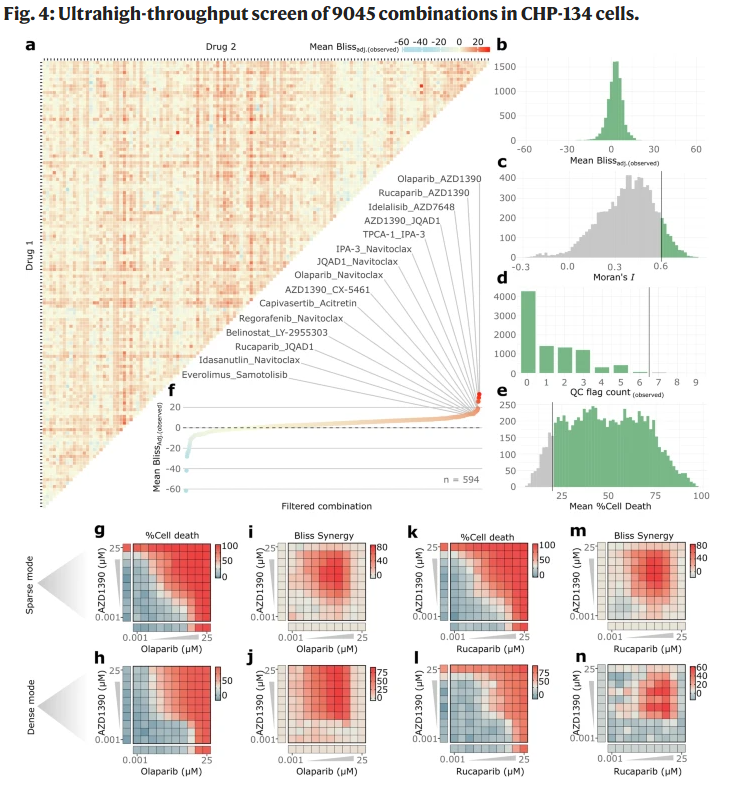
图 4|超大规模药物组合筛选结果与候选协同组合。
讨论
该研究表明,通过将先进实验自动化技术与机器学习推断深度融合,药物组合筛选可以突破传统在规模与分辨率上的双重限制。Combocat 不仅提供了一个高效、可扩展的技术框架,更重要的是以开源形式向社区开放,为不同疾病模型和实验体系的快速部署提供了基础。
从长远来看,这种平台化、社区驱动的策略有望逐步构建覆盖多细胞类型、多药物背景的协同作用图谱,为理性设计联合用药方案提供系统性依据。
整理 | DrugOne团队
参考资料
Wright, W.C., Pan, M., Phelps, G.A. et al. An open-source screening platform accelerates discovery of drug combinations. Nat Commun 16, 11005 (2025).
https://doi.org/10.1038/s41467-025-66223-8

内容为【DrugOne】公众号原创|转载请注明来源
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢