PK-Sim学习笔记
过去二十年,临床药理与定量药理的核心使命始终围绕一个问题展开:如何在人体试验之前,尽可能准确地预测药物在真实患者中的疗效与安全性。
从 PPK到PBPK 到 QSP,从 MIDD 到 in silico trial,临床药理人员不断引入更复杂的模型、更丰富的数据,但现实并不总是理想,许多在模型中“看起来正确”的决策,最终仍然倒在了临床阶段。
最近,两篇具有代表性的综述工作从不同维度给出了一个高度一致的信号:问题并不在于模型不够复杂,而在于我们是否真正把药物“放进了人体系统中去评估”。
一篇文章从“因果性疾病模型、虚拟患者和数字孪生”的角度,讨论了 in silico 临床试验如何重塑药物研发决策[1];另一篇则提出“可编程虚拟人”的概念,试图在虚拟人体内端到端评估从未出现过的新分子[2]。
本推文将结合这两项工作,总结简要阐述下目前AI推动虚拟人群的建立及应用情况。
因果疾病模型
随着大规模患者多组学数据的积累,慢性和复杂疾病的计算建模取得了显著进展。研究人员通过整合遗传、转录、蛋白、代谢及免疫表型等多维数据,并结合临床信息,对疾病进行系统性刻画。
疾病建模主要带来两方面价值:
揭示疾病异质性:将患者划分为具有共同病理机制的亚群;
识别关键致病通路与治疗靶点:明确在特定患者亚群中被异常调控的分子网络。
人工智能被引入模型计算极大的加速了整个工作的进程。在前期基础上,AI用于评估每一个异常基因或蛋白对整个疾病系统的影响强度,最终构建出以“主调控因子”为核心的因果性疾病互作网络。通过对该网络进行计算扰动,可以在理论上模拟药物作用于特定靶点后的整体生物学效应,并为联合治疗策略提供线索。
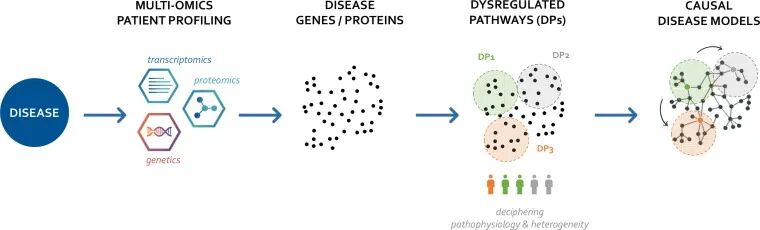
AI强化的QSP模型
定量系统药理学(QSP)通过机制模型整合疾病生物过程与药物的药代动力学和药效学信息,在药物发现和开发中被广泛应用。QSP 在早期研发阶段可用于靶点和生物标志物筛选,在后期则可用于预测不同给药方案下的临床反应。
研究人员指出,QSP 模型的构建和验证过程复杂,对生物学、药理学和计算建模能力要求较高,但其方法学已逐步获得监管机构认可。
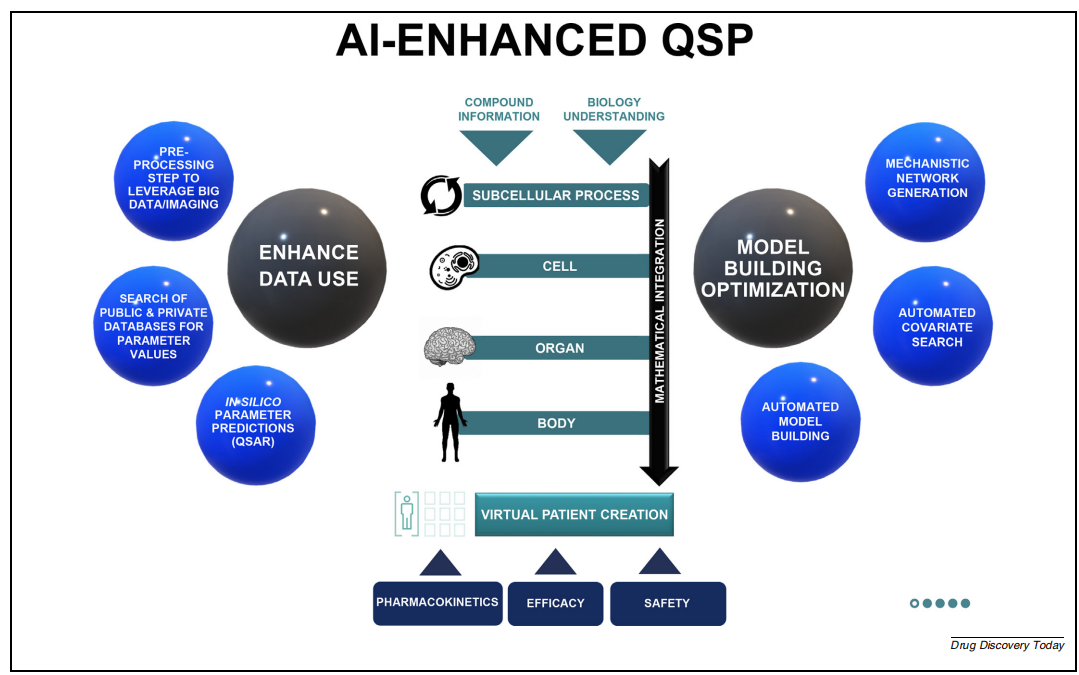
近年来,人工智能显著增强了 QSP 模型的能力,具体体现在:
更高效地整合多来源、多模态数据;
自动化模型构建、参数估计和协变量筛选;
构建大规模虚拟患者群体,用于模拟人群异质性。
此外,研究人员认为,自上而下的机制模型与自下而上的智能体模型具有互补性,二者结合有助于在细胞、组织和整体层面更真实地模拟药物作用过程。
这个前段时间在PSP上也发表了一篇AI-QSP的Tutorial [3],感兴趣的也可以去阅读学习下(QSP-Copilot: An Al-Augmented Platform for AcceleratingQuantitative Systems Pharmacology Model Development)。
虚拟患者与数字孪生
虚拟患者是通过整合多个真实患者数据构建的计算模型,能够在不涉及隐私风险的前提下反映疾病的真实复杂性。这类模型已被用于构建虚拟对照组,特别适用于病程高度可预测或伦理上难以设置安慰剂对照的疾病。
数字孪生最初源于工程领域,在医学中通常用于模拟特定器官或组织,结合高分辨率医学影像和物理特性,生成患者特异性的模型。数字孪生可用于开展现实中难以实施或风险较高的“虚拟实验”,并已在部分医疗器械评估中取得成功。
研究人员强调,无论是虚拟患者还是数字孪生,其可信度均依赖于严格的模型验证,包括:
模型假设与结构的透明性;
与真实临床研究结果的一致性验证;
对目标患者人群特征的充分刻画。
此外,基于虚拟患者或历史数据构建的“外部对照组”正在成为替代传统对照的重要补充手段,尤其适用于伦理限制较高的研究场景。
所以今年11月纽约大学写了一篇新的综述,提出需要一种全新的虚拟人体模型:不仅能模拟已知药物,还能预测从未出现过的新分子在人体中的生理效应,并支持反向设计以恢复健康状态。
可编辑的虚拟人(PVH)
1. 什么是可编辑的虚拟人?
PVH 被定义为一种能够在人体生理学框架下,端到端模拟新分子从给药到临床结局全过程的计算平台。与传统线性药物研发流程不同,PVH 直接以患者层面的疗效与安全性为优化目标,从而在理论上消除靶点发现、先导优化、动物实验与临床试验之间的层层转化损失。
研究人员将这一过程类比为生成式 AI:以“疾病状态的虚拟人体”和“健康参考人体”为输入提示,反向生成能够将疾病状态推回健康状态的分子。
其提出的原因主要是:数字孪生模型虽被提出用于模拟人体中药物行为,服务于临床试验设计与个体化用药。但这类模型严重依赖已有临床或真实世界数据,对于全新的化学实体而言,缺乏必要的参数与先验信息,难以在药物发现早期发挥作用。
两者对比如下:
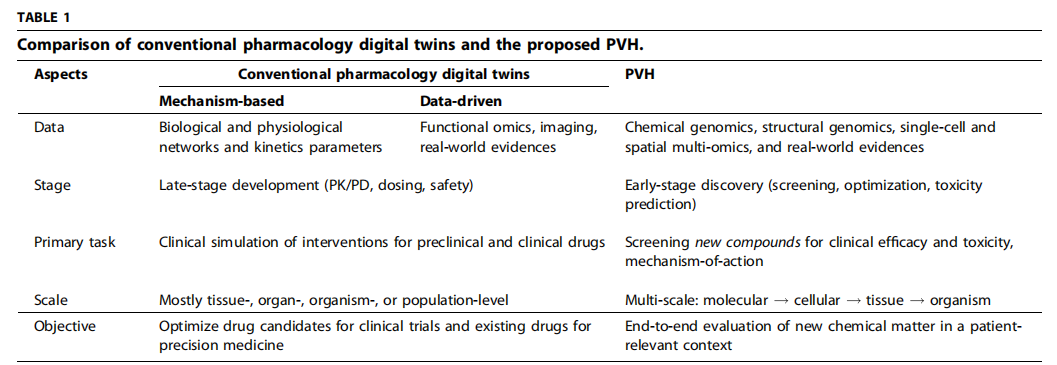
PVH的工作流以及应用
传统药物发现模式在面对复杂疾病时已显现明显瓶颈,而可编程虚拟人代表了一种潜在的范式转变:从以中间指标为导向,转向以人体整体生理结局为核心目标。
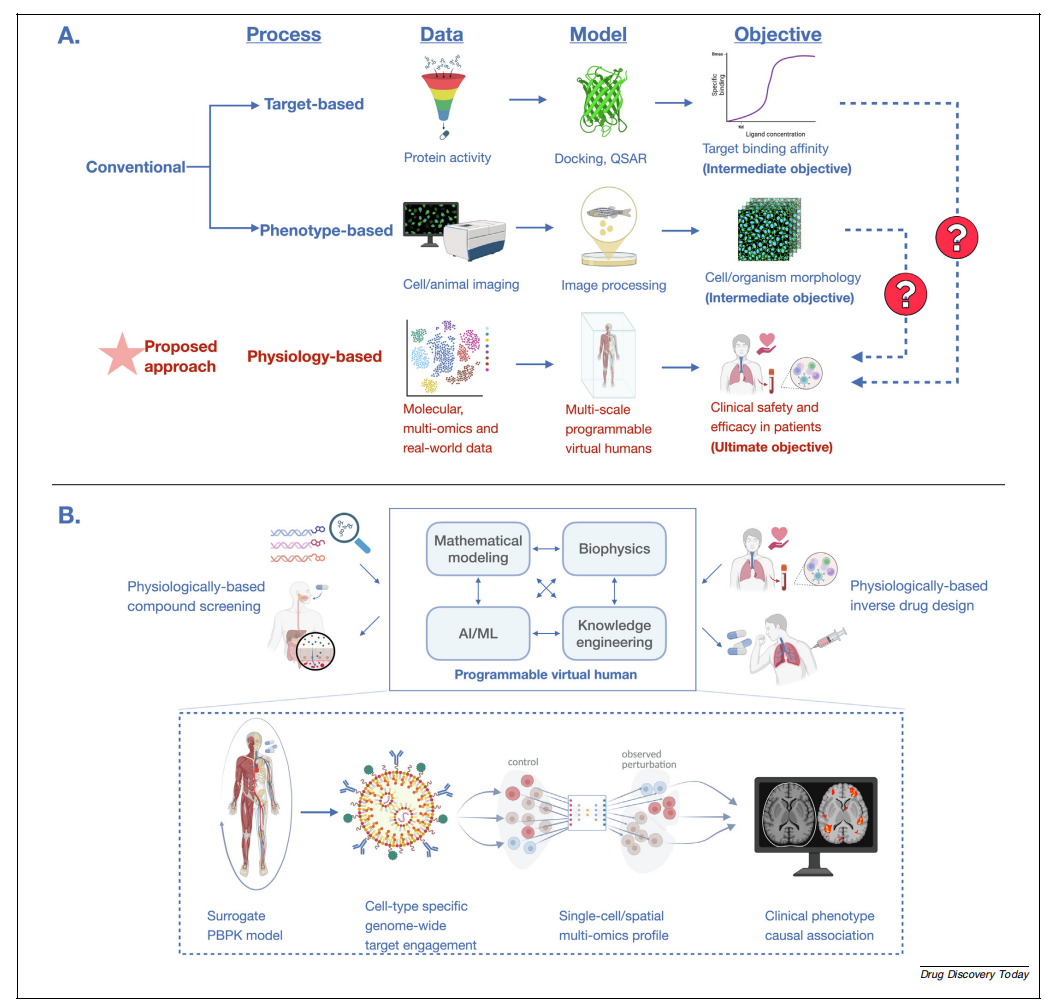
其应用场景如下:
1. 模拟未知分子在人体中的命运
PVH 的核心任务之一,是预测新分子的药代动力学与药效学行为。
传统 PBPK 和定量系统药理模型基于微分方程,依赖明确的参数,难以泛化到未知分子;
通过将机器学习与 PBPK、QSP 结合,可提升对新化学结构的预测能力;
物理信息神经网络等方法,通过引入生物物理约束,在数据稀缺条件下提升泛化性与可解释性。
在分子层面,PVH 还需预测新化合物与全基因组蛋白的结合行为,包括结合构象、动力学特征以及功能选择性,从而更真实地反映药物在体内的多靶点效应。
2. 多层级细胞状态建模
PVH 必须能够在不同遗传与环境背景下,准确模拟细胞对分子扰动的响应。单细胞组学技术的发展,使得从 DNA、RNA、蛋白、代谢物到细胞表型的多层级刻画成为可能。
研究人员指出,单一组学只能反映局部信息,必须通过多模态深度学习将不同层级的数据整合为统一表示,以模拟生物信息在不同层级之间的传递过程,从而预测基因—环境—表型关系。
3. 多器官与系统层面的整合
人体是一个高度耦合的多器官系统,局部异常可通过复杂网络影响全身功能。PVH 通过整合空间组学、多器官模型和细胞间通信机制,能够模拟疾病在不同器官间的相互作用,为理解复杂疾病提供系统性视角。
4. 预测新扰动下的临床反应
通过扰动功能基因组学、图像型表型分析以及微生理系统数据,PVH 可以学习“扰动—响应”关系,并推断未知药物在人体中的潜在临床效应。
研究人员强调,尽管这些数据并非直接来源于患者,但结合 PBPK、多组学和生成式 AI 技术,有望在一定程度上弥合模型系统与人体之间的转化差距。
参考资料
[1] Moingeon P, Chenel M, Rousseau C, Voisin E, Guedj M. Virtual patients, digital twins and causal disease models: Paving the ground for in silico clinical trials. Drug Discov Today. 2023 Jul;28(7):103605. doi: 10.1016/j.drudis.2023.103605
[2] Wu Y, Bourne PE, Xie L. AI-powered programmable virtual humans toward human physiologically-based drug discovery. Drug Discov Today. 2025 Nov;30(11):104497. doi: 10.1016/j.drudis.2025.104497
[3] Saini A, Farnoud A. QSP-Copilot: An AI-Augmented Platform for Accelerating Quantitative Systems Pharmacology Model Development. CPT Pharmacometrics Syst Pharmacol. 2025 Nov;14(11):1775-1786. doi: 10.1002/psp4.70127
扫码添加好友


PK Sim学习笔记
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢