

医学
Medicine


在精准肿瘤学领域,基因组分析通常是指导临床治疗决策的首要依据。然而,许多癌症,尤其是一些侵袭性白血病类型,目前仍缺乏明确的、具有临床可干预性的基因组变异。在这种情况下,直接对肿瘤细胞进行体外药物敏感性检测,已成为一种重要的补充策略。
然而,传统药敏检测方法受限于较长的药物孵育周期、较高的样本与试剂需求量以及复杂的操作流程,难以广泛应用于临床实践。更重要的是,这类方法大多仅能反映细胞群体的整体反应,无法捕捉与药物敏感性密切相关的单细胞特征,例如肿瘤内异质性、蛋白质表达的空间分布及细胞形态变化。因此,面对儿童T细胞急性淋巴细胞白血病等治疗选择有限、预后仍有改善空间的疾病,开发一套快速、自动化、具备单细胞解析能力的药物敏感性预测平台,具有重要的临床意义与应用价值。
近日,来自美国犹他大学的科学团队在Cell Press细胞出版社旗下期刊Med上在线发表了一篇题为“μPharma: A Microfluidic AI-driven Pharmacotyping Platform for Single-cell Drug Sensitivity Prediction in Leukemia”的重磅研究,提出了一种名为μPharma的新型药敏预测平台。该平台旨在通过检测治疗前的特定生物标志物,无需对细胞进行长期药物暴露,即可在数小时内实现对单细胞药物敏感性的预测。


▲长按图片识别二维码阅读原文
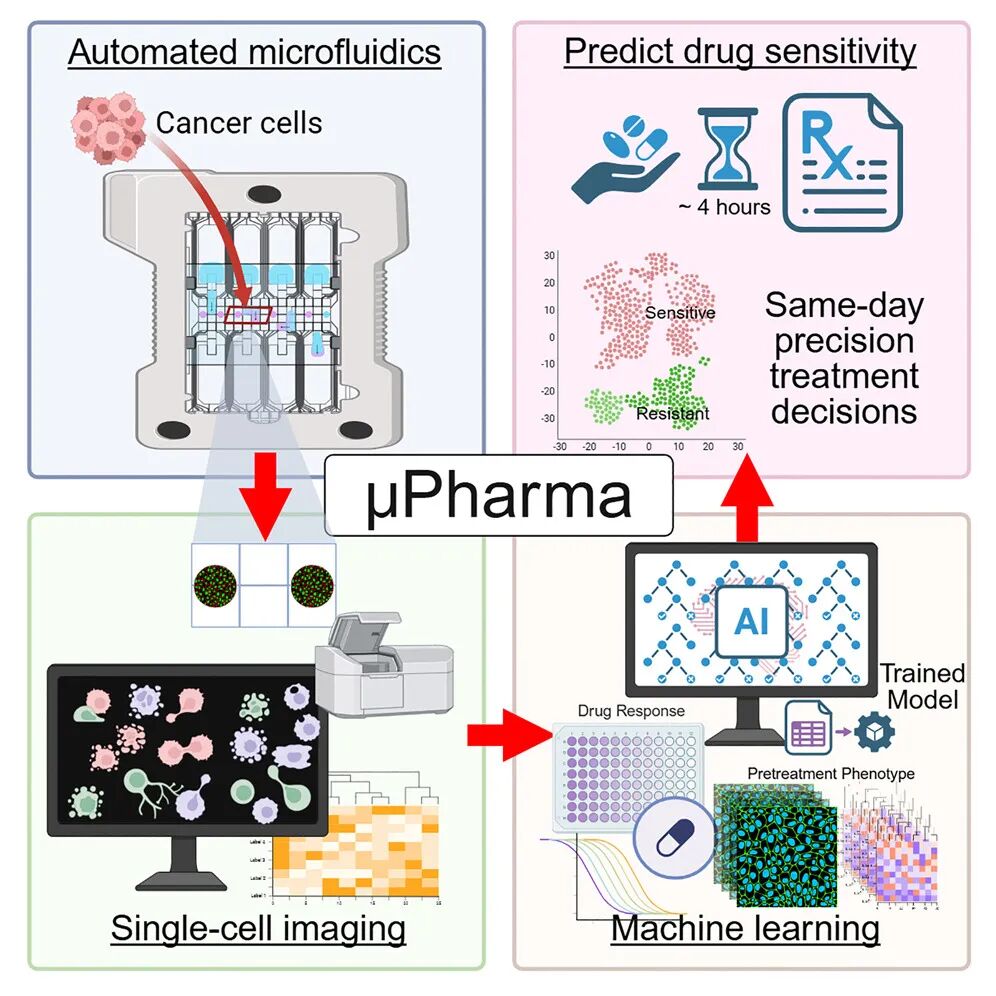
μPharma平台的核心架构包含三个紧密衔接的分析模块。首先是专为悬浮细胞设计的全自动数字微流控免疫荧光检测系统。该系统通过在芯片上集成微电极阵列,能够精准操控纳升至微升尺度的液滴运动,无需依赖物理管道或泵阀装置,即可在亲水区域形成被称为“虚拟纳米孔”的微反应环境。每个微孔可容纳约1500个细胞,反应体积仅约300纳升,从而显著降低试剂消耗并减少操作误差。在该模块中,细胞固定、透化、封闭及多重抗体染色等步骤均可自动完成。检测结束后,经由荧光扫描可获得单细胞分辨率的多通道图像,进而量化目标蛋白的表达水平、磷酸化状态及其在细胞内的空间分布特征。其次,平台构建了一个与微流控检测相匹配的批量药敏数据库。该数据库通过传统体外剂量反应实验,测定各样品的半数致死浓度,并依据阈值将样本划分为药物敏感型或耐药型,为后续模型训练提供基准标签。最后,平台利用机器学习算法整合前两个模块的输出信息。通过从单细胞图像中提取涵盖蛋白强度、空间分布、形态学指标及其交互关系在内的多维特征,并结合批量药敏标签,训练出高效的预测模型。模型训练完成后,仅需对新增样本进行4小时的微流控检测,即可基于所提取的特征实现快速、自动化的药物敏感性预测,无需再次进行长期药物孵育实验。
为实现悬浮细胞在微流控芯片上的稳定分析,研究团队开发了一种无需额外化学试剂的细胞固定策略。通过对多种表面修饰方法进行比较,发现采用缓冲液沉降法(即依赖重力使细胞自然吸附于亲水性位点)与高浓度聚-D-赖氨酸涂层均能实现较高的细胞保留率,且两者效果相当。重要的是,缓冲液沉降法避免了聚阳离子材料可能引发的T细胞活化或表型改变,更具生物学惰性。为进一步验证该策略的可靠性,研究选取了两种磷酸化LCK基础表达水平不同的T-ALL细胞系,并按不同比例混合后进行测试。实验结果显示,即使经过包括多次液滴交换在内的完整微流控处理流程,细胞在芯片上的保留率仍能稳定保持在85%以上。此外,通过对比数字微流控检测技术与传统磷酸化流式细胞术所测得的pLCK信号强度,两者呈现高度一致的相关性。这一结果不仅确认了该固定方法能有效维持细胞原有的蛋白表达与磷酸化状态,也同时表明微流控系统在显著减少细胞用量及试剂消耗的前提下,仍能获得与常规方法可比的数据质量。
为验证平台的预测能力,研究以T-ALL细胞为模型,选取了分别靶向激酶LCK和抗凋亡蛋白BCL2的两种临床药物——达沙替尼与维奈克拉进行分析。首先,研究团队在七株T-ALL细胞系中通过数字微流控检测同步量化了LCK及其磷酸化形式(pLCK)、BCL2及其磷酸化形式(pBCL2)的表达水平。与此同时,通过传统的体外药物敏感实验明确了各细胞系对上述两种药物的反应特征。结果表明,对达沙替尼敏感的细胞系普遍表现出显著的pLCK高表达,而对维奈克拉敏感的细胞系则呈现较高的pBCL2水平。进一步的线性回归分析显示,pLCK表达与达沙替尼的半数抑制浓度呈负相关,pBCL2表达与维奈克拉的半数抑制浓度亦呈现类似趋势。值得关注的是,pBCL2作为维奈克拉敏感性的预测标志物,此前在T-ALL中尚未见系统报道。在单细胞层面,受试者工作特征曲线分析证实,基于pLCK或pBCL2的信号强度能有效区分药物敏感与耐药的细胞亚群。此外,同一细胞系内单细胞标志物表达的异质性,提示即使在克隆来源的细胞群中,也可能存在具有不同药物反应特性的细胞亚群,这为理解肿瘤异质性与治疗反应差异提供了线索。
为验证磷酸化蛋白与药物敏感性的关系在更接近临床实际的模型中是否依然成立,研究进一步将微流控检测系统应用于14例经充分表征的T-ALL患者来源异种移植模型。分析结果显示,达沙替尼敏感PDX样本中pLCK的平均表达强度显著高于耐药样本。除一例特殊情况外,维奈克拉敏感的PDX样本也普遍表现出更高的pBCL2水平。该例外样本SJ7虽然对维奈克拉敏感,但其pBCL2仅呈中等表达,提示其可能代表一类具有独特生物学特征的T-ALL亚型。基于单细胞数据的ROC分析再次表明,pLCK与pBCL2的表达水平能够有效区分PDX来源的敏感与耐药细胞群体,进一步证实了磷酸化蛋白在临床相关模型中对治疗反应具有预测价值。
为进一步提高预测准确性,研究构建了基于XGBoost算法的机器学习模型。该模型利用从单细胞图像中提取的428项定量特征进行训练,并采用严谨的旋转交叉验证策略来评估其稳定性与泛化能力。在达沙替尼与维奈克拉的敏感性预测任务中,模型均表现出优秀的判别性能,其平均ROC曲线下面积达到较高水平。通过SHAP可解释性分析对特征重要性进行解析发现,对达沙替尼敏感性最具预测力的特征主要包括pLCK表达强度的下四分位数、位于细胞外周区域的pLCK平均强度,以及pLCK平均强度与细胞形态参数构成的交互项。而在维奈克拉敏感性预测中,关键特征则涉及pBCL2表达强度的上四分位数,以及细胞边缘区域BCL2的最低表达水平。这些结果共同表明,蛋白质的表达丰度、其在细胞内的空间分布特点、表达水平的异质性以及细胞形态特征,均与肿瘤细胞的药物敏感性存在密切关联。
研究进一步通过UMAP降维方法,对关键SHAP特征进行可视化,直观呈现了这些特征如何捕获与药物敏感性相关的单细胞模式及肿瘤内异质性。在降维空间中,细胞主要按敏感与耐药表型形成不同的聚集区域,同时也呈现明显的样本特异性分布模式。当将各样本的细胞投影到该空间时,可以观察到即使在同一批被归类为敏感或耐药的样本内部,也存在分布于相反表型区域的细胞亚群,清晰揭示了肿瘤内存在的异质性。例如,对达沙替尼敏感的样本SJ65中,绝大多数细胞位于敏感区域,但仍可识别出一小部分细胞散布于耐药区域。
综上所述,μPharma平台通过将自动化微流控单细胞蛋白检测与机器学习分析相结合,实现了基于生物标志物的快速、单细胞精度的药物敏感性预测,显著突破了传统药敏检测的技术局限。该研究不仅进一步验证了pLCK与达沙替尼敏感性之间的关联,更首次在T-ALL中确立了pBCL2作为维奈克拉疗效预测标志物的潜在价值。通过融合蛋白空间分布与细胞形态等多维度特征,模型的预测能力得到有效增强,而其单细胞分辨率的特点,也直观揭示了肿瘤内部的异质性,为识别和理解耐药细胞亚群提供了新的视角。

相关论文信息

论文原文刊载于Cell Press细胞出版社
旗下期刊Med,
点击“阅读原文”或扫描下方二维码查看论文

▌论文标题:
μPharma: A microfluidic, AI-driven pharmacotyping platform for single-cell drug sensitivity prediction in leukemia
▌论文网址:
https://www.sciencedirect.com/science/article/abs/pii/S2666634025003939
▌DOI:
https://doi.org/10.1016/j.medj.2025.100966

▲长按图片识别二维码阅读原文
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢