
01
遇见/背景
手性α-羟基酮是药物和精细化学品合成中的关键中间体,其高效、高选择性的生物催化合成具有重要意义。利用2,3-丁二醇脱氢酶还原邻二酮或氧化邻二醇是生产α-羟基酮的重要途经,但现有的2,3-丁二醇脱氢酶均存在立体选择性较低的困境,阻碍了以混合型邻二醇为底物,合成手性α-羟基酮。
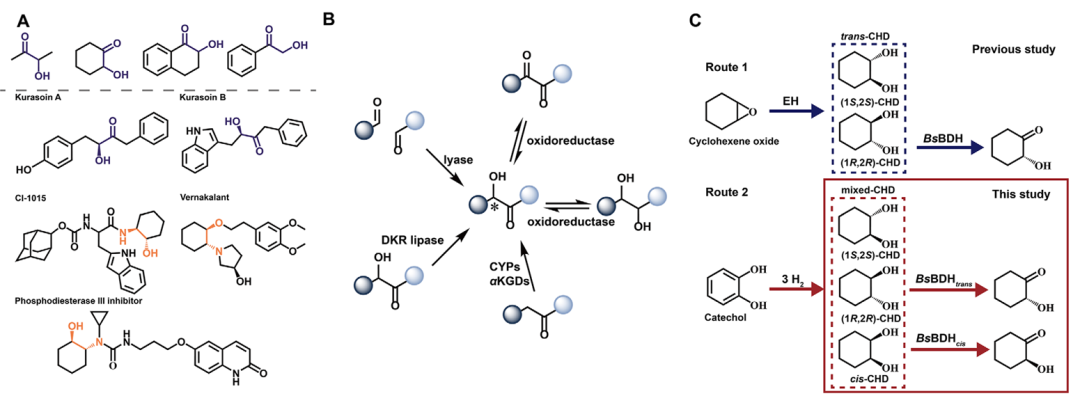
图1 重要的α-羟基酮化合物及其合成路径
2026年1月25日,浙江大学化学工程与生物工程学院于浩然课题组在国际期刊《Advanced Science》发表题为“Protein Language Model-Guided Engineering of a 2,3-Butanediol Dehydrogenase for the Enantioselective Synthesis of Cyclic α-Hydroxy Ketones”的研究论文。
该研究结合蛋白质语言模型和迭代饱和突变对来自枯草芽孢杆菌的2,3-丁二醇脱氢酶(BsBDH)进行改造,提高甚至反转其对1,2-环己二醇的立体选择性。该研究首先通过分子对接与蛋白质语言模型ESM-1v识别出影响立体选择性的关键残基。随后,该研究提出了PASS热稳定性改造策略,该策略通过分析结构柔性与同源序列来源,显著提升了酶的热稳定性设计效率,其真阳性率高达88.2%。以热稳定变体6M2为基础,在关键位点进行迭代饱和突变,成功获得两种具有高度立体选择性的突变体:对trans-1,2-环己二醇(trans-CHD)具有偏好性的变体LTF(ee>99%)与对cis-1,2-环己二醇(cis-CHD)具有偏好性的变体10M(ee>99%)。同时获得了多个催化活性显著提升的突变体,对25种不同底物的催化活性均有提高。分子动力学模拟与非天然氨基酸引入成功揭示了突变体选择性提高和反转的分子机制。本研究表明,蛋白质语言模型引导的迭代饱和突变能够有效实现酶活性与立体选择性的快速优化,为高效、专一性生物催化剂的理性设计提供了新策略。

02
遇见/内容
1、蛋白质语言模型ESM-1v筛选关键残基
该研究结合AlphaFold3预测的蛋白结构与ESM-1v蛋白质语言模型,精准识别出决定BsBDH立体选择性的三个关键残基(F115、L118、Y293)。该研究不仅考虑了ESM-1v零样本预测的结果,同时考虑每个位点突变的多样性,确保初次筛选中的单点突变具备代表性。实验结果表明,零样本预测有效排除了可能导致酶活丧失的有害突变,将实验验证聚焦于高潜力位点,极大提升了筛选效率与成功率。
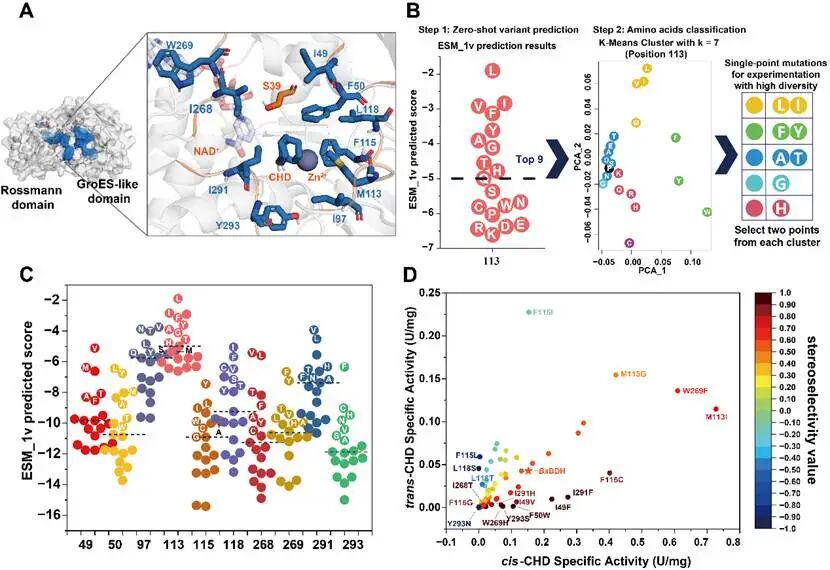
图1 PLM辅助的单点突变预测
2、PASS热稳定性改造策略
该研究首先对野生型序列进行热稳定性改造,为后续立体选择性进化提供一个稳定可靠的蛋白质骨架。为解决传统ΔΔG计算假阳性率高的问题,团队开发了PASS策略,通过分析突变位点的柔性区域并比对嗜热同源蛋白的进化信息,对预测突变进行双重过滤。该方法将热稳定突变体的真阳性率提升至88.2%。随后通过Gibson组合对热稳定性单点突变进行组合,获得了一个热稳定性提升14.8倍的六点突变6M2。
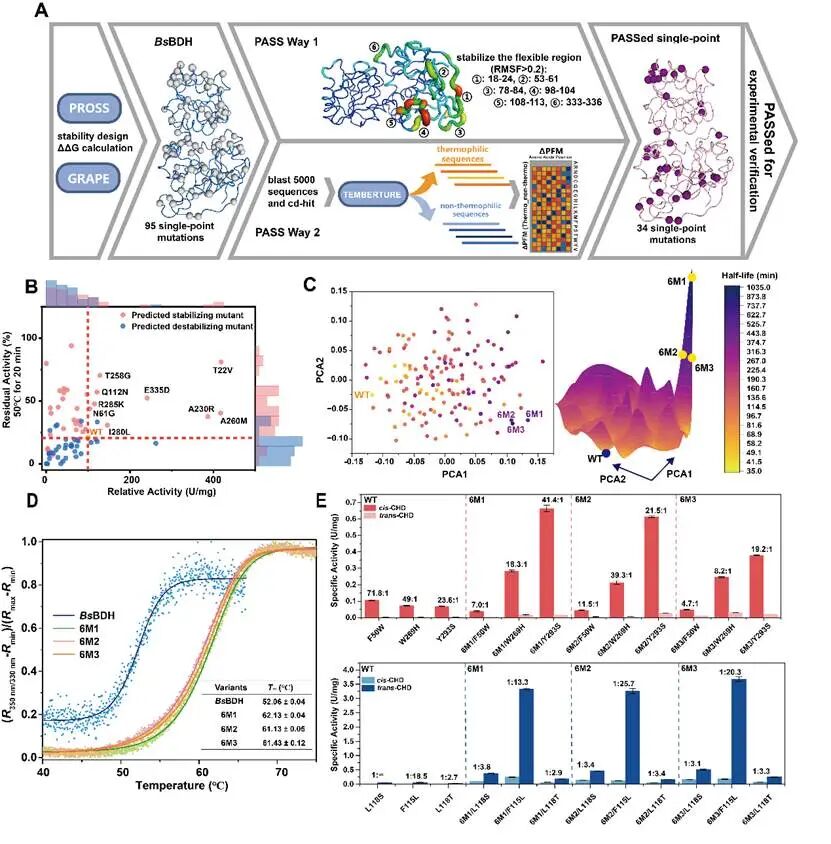
图2 计算设计提高BsBDH的热稳定性
3、关键残基迭代饱和突变提高和反转立体选择性
以热稳定突变体6M2为模板,在关键位点进行完美迭代饱和突变。成功获得了对trans-CHD具有专一性的突变体LTF和对cis-CHD具有专一性的突变体10M,实现了立体选择性的反转及调控。此外,在进化路径中获得两个高催化活性突变体,6M2/F115C/L118F和6M2/F115L/L118M分别对cis-CHD和trans-CHD的催化效率提高了93.10倍和316.85倍,底物谱测定结果表明,高活性突变体对34个底物中的25个提高了催化活性,其中对1,2-二羟基茚满的催化活性提升倍数最为显著,相较于野生型分别提高了1521.1倍和5182.1倍。
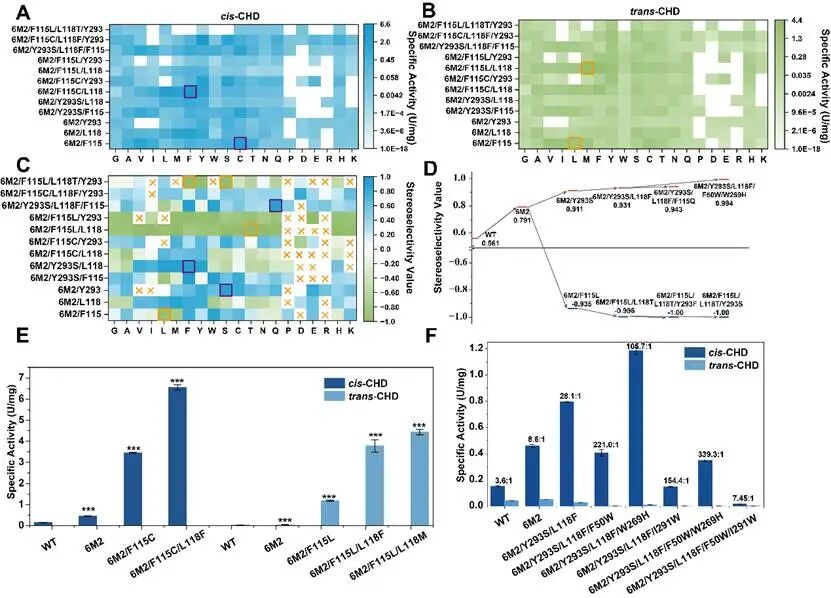
图3 迭代饱和突变改造BsBDH
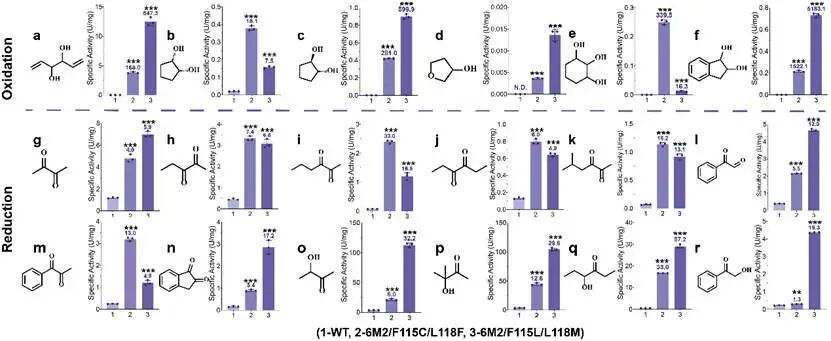
图4 高催化活性突变体的底物谱测定
4、全细胞催化转化混合型1,2-环己二醇
将BsNOX和BsBDH或选择性突变体(10M和LTF)共转化,构建辅酶再生的全细胞催化体系。全细胞催化结果表明,10M对cis-CHD具有高选择性,能以混合型1,2-CHD为底物合成S-HCH,ee值大于99%;LTF对trans-CHD具有高选择性,能以混合型1,2-CHD为底物合成R-HCH,ee值大于99%。
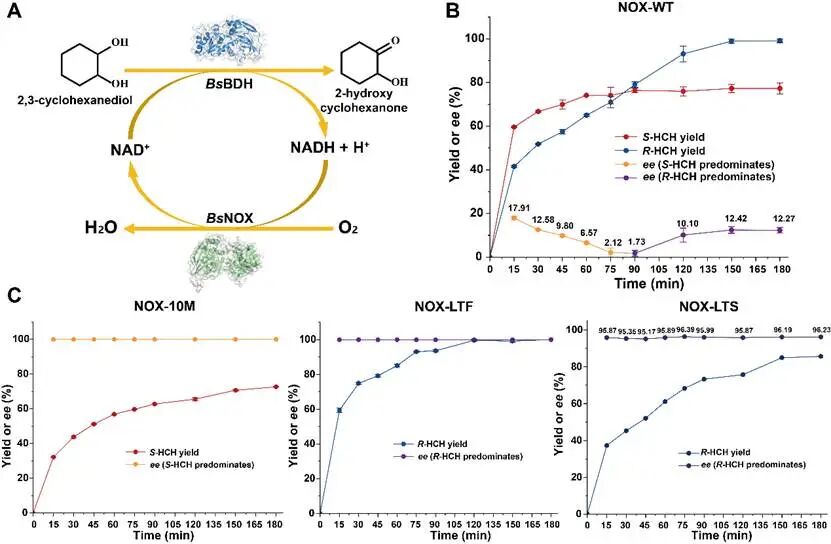
图5 全细胞催化合成手性2-羟基环己酮
5、分子动力学模拟揭示突变体性能提升机制
该研究通过分子动力学模拟,深入解析了突变体6M2、10M及LTF的结构与功能关系。通过模拟发现,热稳定突变体6M2通过形成新的氢键网络与疏水相互作用,显著提升了结构刚性。对于立体选择性突变体10M和LTF,分析显示其结合口袋的几何形状改变导致底物攻击角度差异,进而决定了对cis-CHD或trans-CHD的选择性偏好。此外,通过伞状采样,揭示了产物释放通道的疏水作用调控机制,阐明了突变如何通过影响产物释放能垒,实现立体选择性的精准控制。
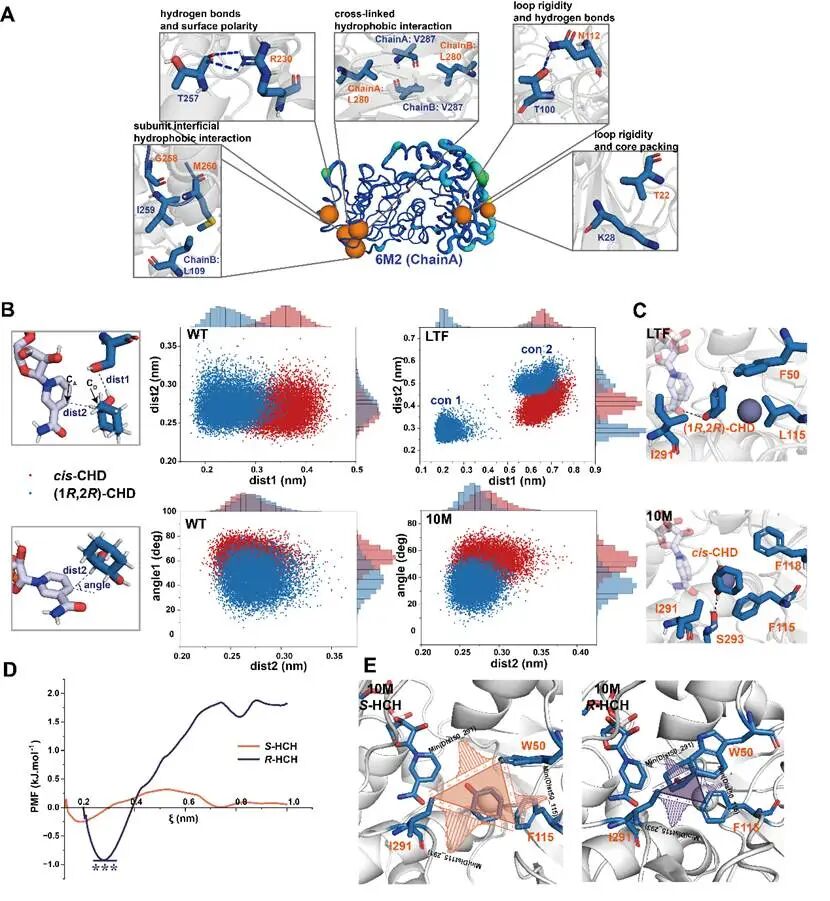
图6 分子动力学模拟解析突变体
6、引入非天然氨基酸揭示关键残基的功能机制
该研究进一步通过基因密码子扩展技术,在BsBDH的关键位点F50和L118引入卤代苯丙氨酸等非经典氨基酸。实验表明,在位置50引入2,5-二氯苯丙氨酸能显著扩大产物释放通道,使催化效率提升214倍;而在位置118引入3-溴苯丙氨酸可将立体选择性从25:1提升至71.9:1。该研究直接验证了残基空间取向和卤键作用在调控酶活性和选择性中的关键角色,为酶机制解析提供了新工具。
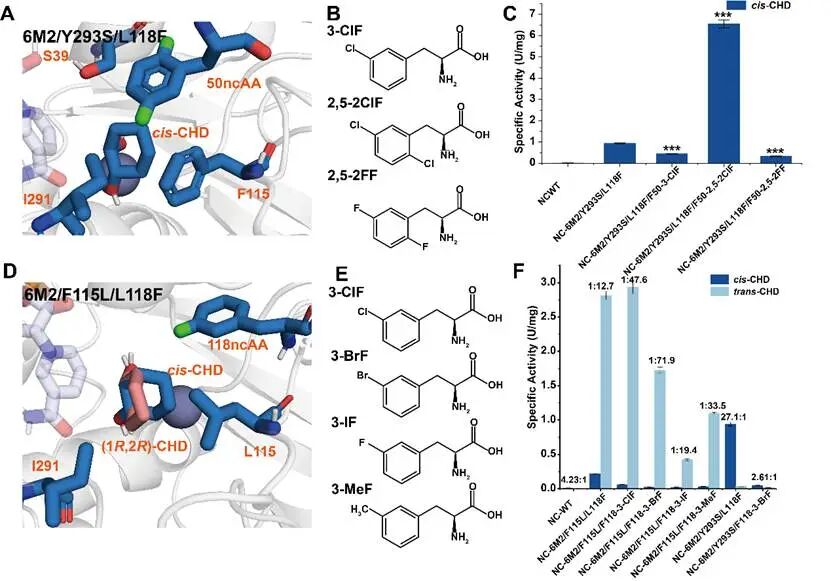
图7 引入非天然氨基酸重构结合口袋和底物释放通道
该研究通过蛋白质语言模型、迭代饱和突变和非天然氨基酸引入,成功改造了BsBDH并解析了其调控机制。通过蛋白质语言模型ESM-1v精准识别关键残基,结合创新的PASS策略将热稳定性改造真阳性率提升至88.2%。基于此开发的立体选择性突变体LTF和10M,其底物专一性高达ee>99%,活性最高提升5183倍。研究进一步通过分子动力学模拟与非经典氨基酸嵌入技术,阐明突变通过调控底物攻击角度与产物释放通道实现催化性能突破。该研究为α-羟基酮的规模化生物制造提供了高效、绿色的催化平台。
浙江大学化学工程与生物工程学院硕士研究生丁豪特和浙大科创中心生物与分子智造研究院江玲研究员为共同第一作者,通讯作者为浙江大学化学工程与生物工程学院于浩然研究员。该研究得到浙江省“尖兵领雁”研发攻关项目、国家自然科学基金等支持。
03
遇见/致谢
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢