COVID-19大流行极大地推动了针对严重急性呼吸综合征冠状病毒2(SARS-CoV-2)以及用于病毒防控的人类蛋白的治疗干预措施的开发,涉及众多潜在药物和数千名参与临床试验的患者。这些协同努力已在抗病毒药物的发现与开发方面取得了显著进展。
2026年2月25日,山东大学、韩国化学技术研究所及青岛大学的研究团队在《Signal Transduction and Targeted Therapy》上发表综述文章,题为“Antiviral drug discovery and development: challenges and future directions”,其中韩国化学技术研究所的Meehyein Kim与山东大学的刘新泳、展鹏为共同通讯作者。

文章呈现了一份详尽的抗病毒药物开发时间线,追溯了从早期病毒抑制剂到现代广谱抗病毒制剂的发展历程。概述了抗病毒药物发现领域的当前进展状况,涵盖了基于靶点的策略、基于创新机制的方法以及药代动力学优化。此外,探讨了从COVID-19及其他传染病中获得的经验所带来的挑战与未来前景,包括人工智能策略的知识、药物化学工具的利用以及纳米技术应用的进展。
目录
背景
抗病毒药物发展与药物发现基本原理
抗病毒药物发展
药物发现的基本原理
基于结构的抗病毒药物
化合物库
化合物筛选
结构引导的化合物优化
共价结合策略
通过过渡态类似物设计抗病毒药物
基于拓扑结构的抗病毒药物设计
新型作用机制的药物设计
多特异性策略
靶向病毒结构蛋白
用细胞器靶向药物调控病毒
靶向细胞杀伤激活分子
基于性质的药物设计
溶解度优化
成盐
降低细胞毒性
靶向药物递送
前药策略
新兴技术推动药物发现领域
药物化学
人工智能驱动的药物设计
纳米技术
核酸药物
总结与展望
背景
自2020年初以来,新型冠状病毒的出现促使全球药物研究人员积极开展抗病毒药物开发。生物技术与制药行业、学术界以及不同专业领域力量的汇聚,对于成功推动药物创新仍然至关重要。由Frank von Delft等人领导的全球性冠状病毒Moonshot合作项目,在短短18个月内就从针对与SARS-CoV-2主要蛋白酶(Mpro)结合的分子的片段筛选,推进到临床候选药物DNDI-6510的确定。截至2024年3月,中国已有七种口服COVID-19药物上市,包括阿兹夫定、奈玛特韦、莫诺拉韦、先诺特韦、氢溴酸氘瑞米德韦、来瑞特韦和阿泰特韦。在此过程中,无数突破性的策略和方法不断涌现,仿佛学者们跨越研究边界齐聚一堂。COVID-19大流行不仅成为一场全球健康危机,也标志着抗病毒药物开发领域的一个关键时刻。本综述系统总结了此次大流行催生的科学突破和技术创新,为后COVID-19时代抗病毒药物开发的战略规划奠定了坚实基础(图1)。
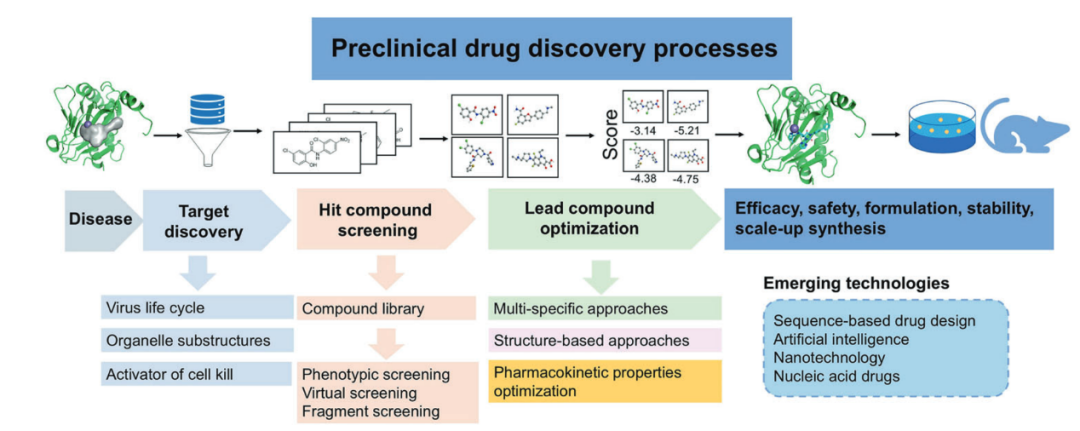
图1 临床前药物发现过程、策略与技术
抗病毒药物发展
新型冠状病毒爆发后,全球研究人员迅速启动了抗病毒药物的研发,并在短时间内取得了显著进展。特别是瑞德西韦和奈玛特韦等药物为抗击COVID-19大流行提供了关键支持。在一项延长阶段的开放性研究和一项回顾性真实世界研究中,共纳入了1974名接受瑞德西韦联合标准治疗的患者,以及1426名仅接受标准治疗的患者。结果表明,瑞德西韦显著降低了死亡风险,并显著提高了患者在28天时出院的概率。
自首个抗病毒药物碘苷获得美国食品药品监督管理局(FDA)批准以来,随后已有超过100种抗病毒药物获得FDA批准。部分抗病毒药物的治疗靶点和临床进展总结如表1所示。
表1 小分子抗病毒药物开发中的治疗靶点与临床进展
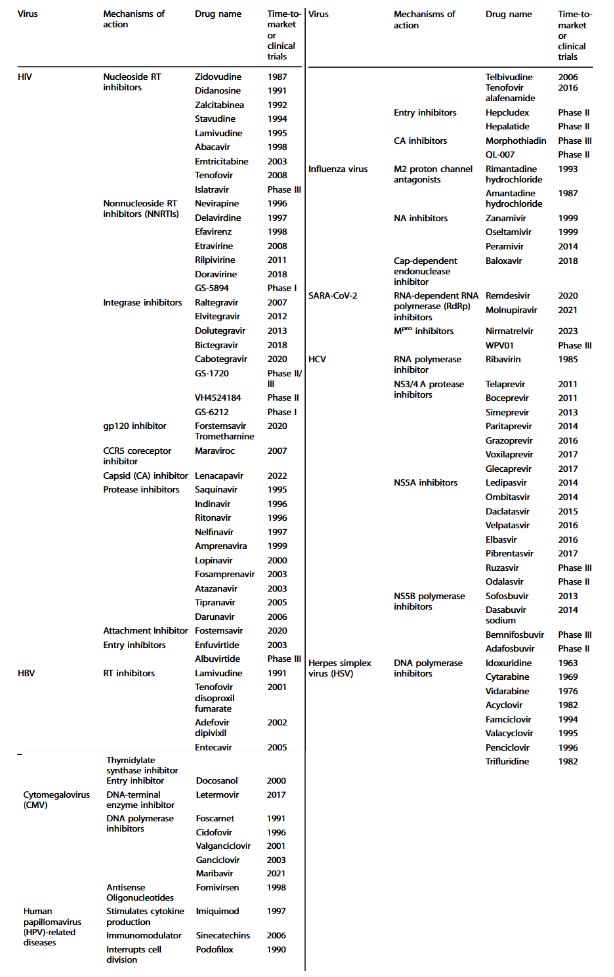
基于结构的抗病毒药物
一旦确定了抗病毒靶点,就可以进行基于结构的药物设计。这涉及使用分子对接和虚拟筛选技术,从大量化合物中快速识别可能与靶蛋白结合的候选分子。通过分析药物与靶蛋白之间的相互作用,可以优化先导化合物的结构,以提高其亲和力、选择性和药代动力学性质。设计能够与靶蛋白上多个位点结合的药物,有助于减少病毒耐药性的产生。此外,通过靶向病毒中保守或跨物种的靶点,基于结构的药物设计有助于开发对多种病毒有效的广谱抗病毒药物。
病毒蛋白通常处于动态构象变化状态。静态晶体结构可能无法全面反映其功能状态,导致预测药物结合位点出现偏差。病毒的快速突变可能导致靶点氨基酸序列改变,这些突变可能使药物结合口袋失效。这些因素极大地限制了基于结构的抗病毒药物发现的发展。HIV融合抑制剂恩夫韦肽通过结合HIV gp41抑制膜融合发挥作用;然而,它需要注射给药,价格昂贵,且由于病毒突变易产生耐药性,这限制了其临床应用。类似地,靶向SARS-CoV-2 S蛋白的单克隆抗体(如bamlanivimab)由于与奥密克戎等变异株相关的S蛋白突变(包括N501Y和E484K)而迅速失去中和活性。
面对这些挑战,基于结构的抗病毒药物发现必须整合冷冻电镜和分子动力学模拟等技术,以阐明病毒蛋白在不同功能状态下的结构,从而促进构象选择性药物的开发。通过多靶点药物设计靶向病毒生命周期的多个阶段(如进入、复制和组装)(图2),有助于降低耐药风险。人工智能算法(如用于蛋白质结构预测的AlphaFold)的应用可以加速药物发现,并克服与传统虚拟筛选方法相关的局限性。
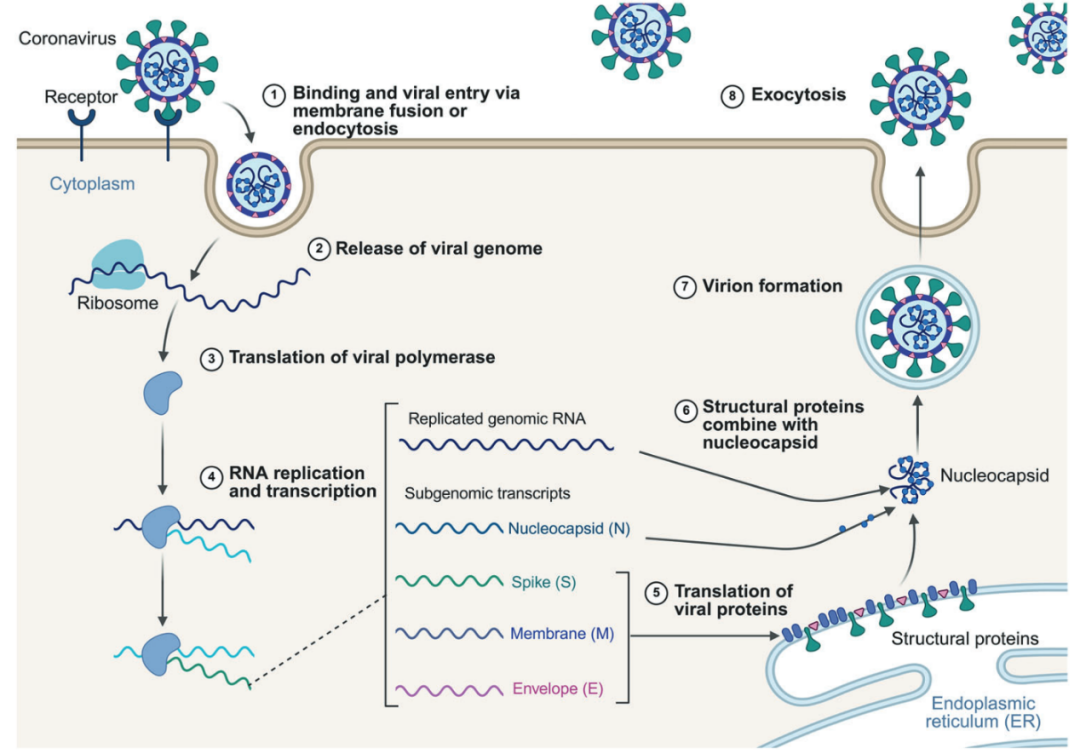
图2 SARS-CoV-2的生命周期
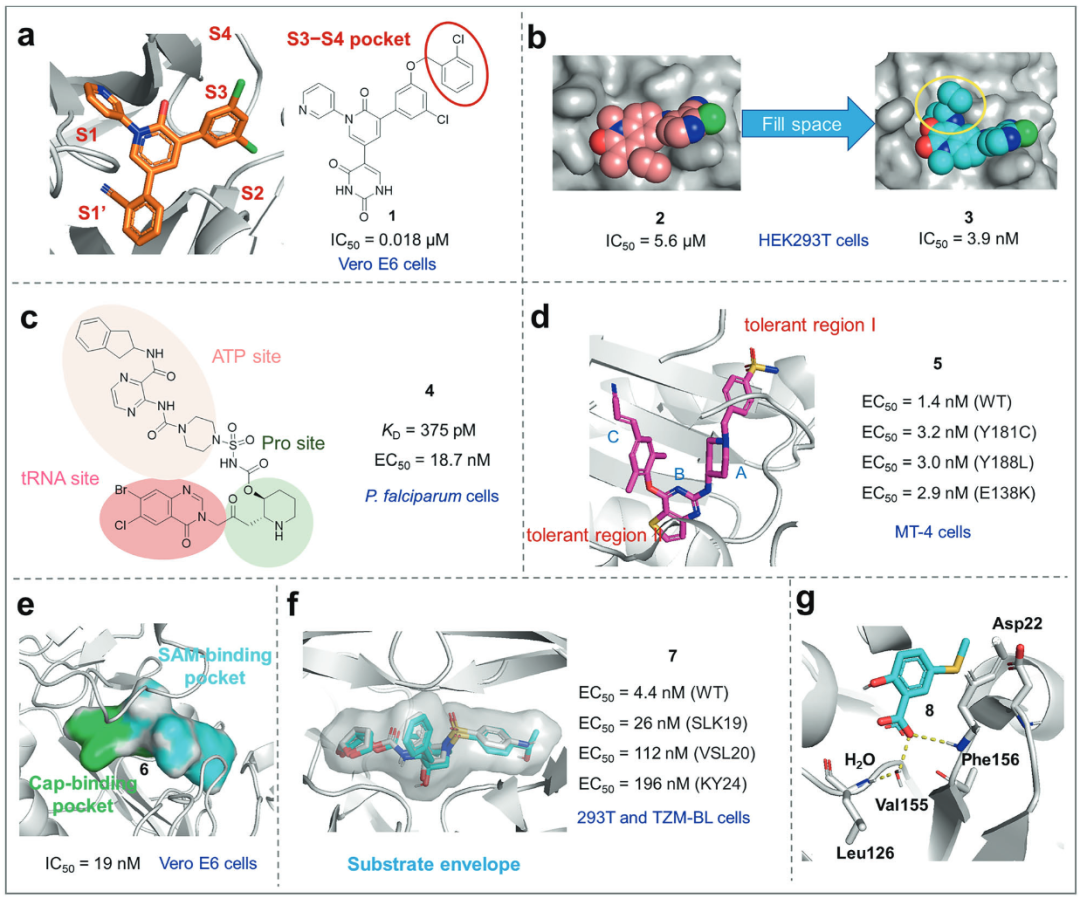
图3 各种结构指导的化合物优化策略
新型作用机制的药物设计
文章介绍了抗病毒药物设计中几种新型作用机制。具体来说,多特异性策略通过同时结合多个目标或效应器来发挥作用,例如将目标蛋白招募到特定细胞器进行降解或将药物定向递送到特定部位以减少副作用。它们虽能提高疗效,但设计和开发更为复杂。靶向蛋白质降解技术包括PROTAC及分子胶。抗体招募分子(ARM)将能招募内源性抗体的分子与靶向病毒表面蛋白的分子结合,激活免疫系统清除病毒感染的细胞。抗体-药物偶联(ADC)利用抗体的靶向性,将高毒性药物精确递送到病毒感染细胞,通过释放药物杀伤细胞。此外,多靶点短肽抑制剂将具有不同作用机制(如抑制病毒融合、拮抗辅助受体)的短肽整合到一个分子中,产生协同增效的抗病毒效果。靶向RNA的降解策略设计能识别并结合特定病毒RNA结构的小分子,通过连接一个能切割RNA的效应分子,实现对病毒RNA的直接降解,从而抑制病毒复制。
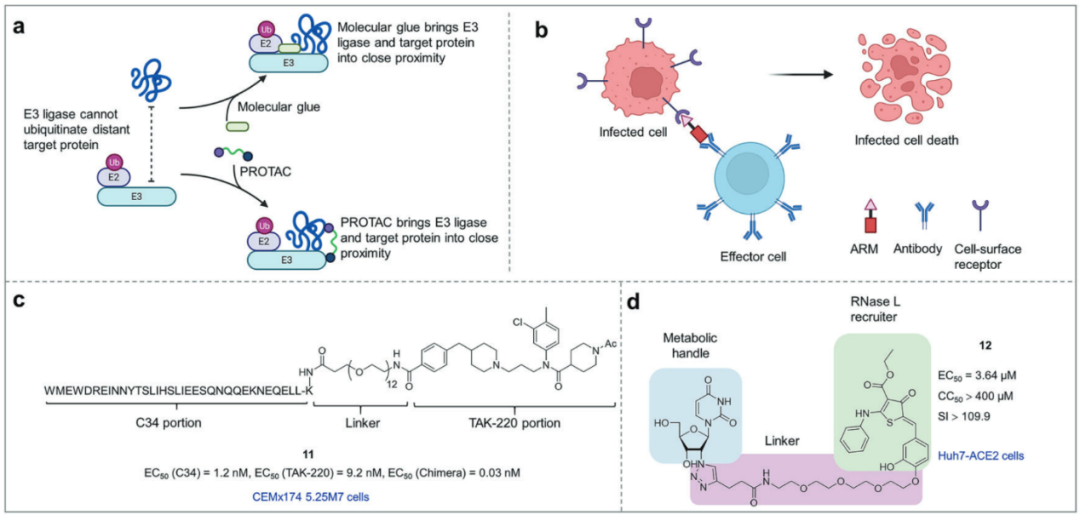
图4 采用多特异性结合策略的抗病毒药物
基于性质的药物设计
基于性质的药物设计涉及对分子和理化属性的细致考量与调控,以优化药物分子的药理学和安全性特征,包括其药效学、药代动力学和毒代动力学性质。成药性通常由药物的需求决定,要求先导化合物在化学上易于合成,并具备理想的ADME特性。此外,这些成药性既包括化合物的物理和化学属性(如溶解性、亲脂性、解离常数和稳定性),也包括其生物学属性。
还要改善药物在体内的行为。具体来说,在靶向药物递送方面,利用靶向分子与特定组织细胞表面的受体特异性结合,实现药物的精准递送,提高局部浓度并降低全身毒性。前药策略是将活性药物进行化学修饰,使其在体外无或低活性,进入体内后在特定条件下(如酶、特定微环境)转化为活性形式。这是一种强大的工具,用于克服药物的吸收、分布、代谢或毒性问题。
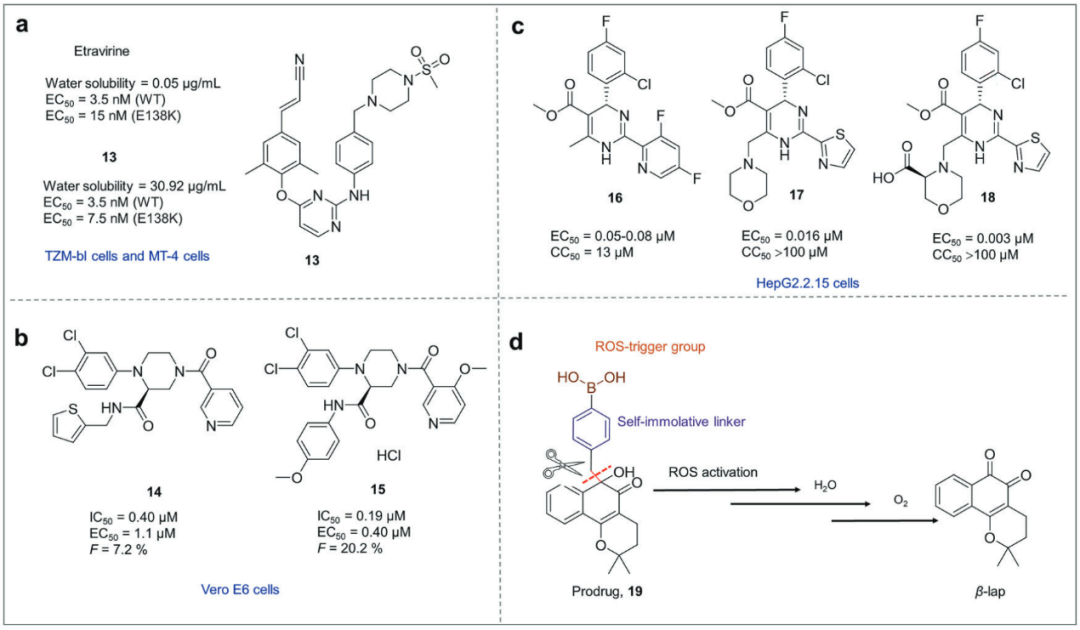
图5 基于性质的药物设计的代表性实例
新兴技术推动药物发现领域
技术的进步为药物发现揭示了新的潜力。具体来说,药物化学提供了更强大、更精准的分子构建工具;人工智能成为理解和预测生物分子世界、加速决策的智能大脑;纳米技术则作为关键的递送和效应平台,解决了药物体内运输和局部作用的难题;核酸药物则开辟了从源头(基因)干预疾病的新路径。这些技术的交叉融合与协同发展,正以前所未有的速度和规模推动着新药的发现。
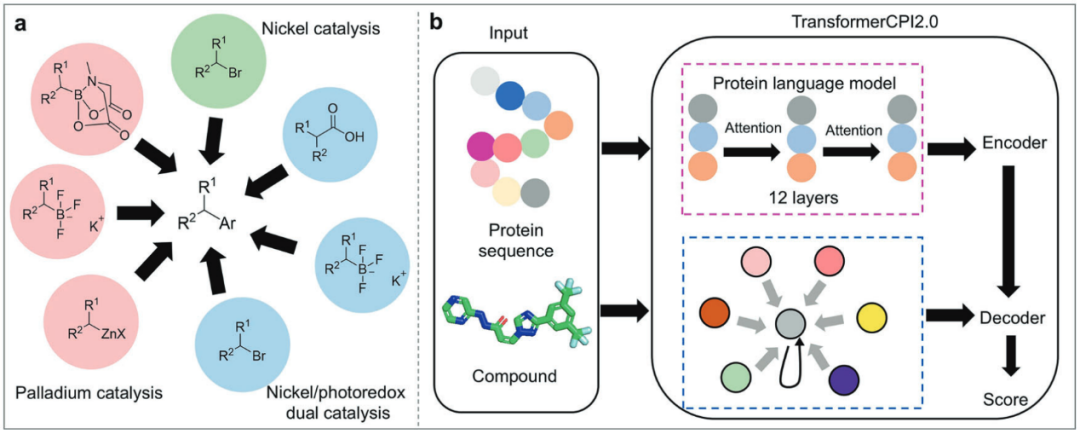
图6 几项新兴技术推动了药物发现领域的发展
总结与展望
目前,仍需要廉价、便利且有效的治疗策略来应对病毒,包括能够解决新突变引起的耐药性的策略。作者总结了抗病毒药物发现的进展和未来趋势,希望能为药物开发提供一些帮助。这些策略包括靶向新位点、利用溶剂暴露区、底物结构、共价结合策略和多价配体的技术。此外,新兴方法如虚拟筛选和靶向蛋白质/RNA降解已被用来遏制耐药性的出现。
药物开发过程不仅涉及技术挑战,还需要制药公司与监管机构尽早沟通。通过从一开始就了解监管要求和审批标准,这些公司可以更好地规划其研究方向和策略,从而避免不必要的调整和延误。
参考链接:
https://doi.org/10.1038/s41392-025-02539-7
--------- End ---------
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢