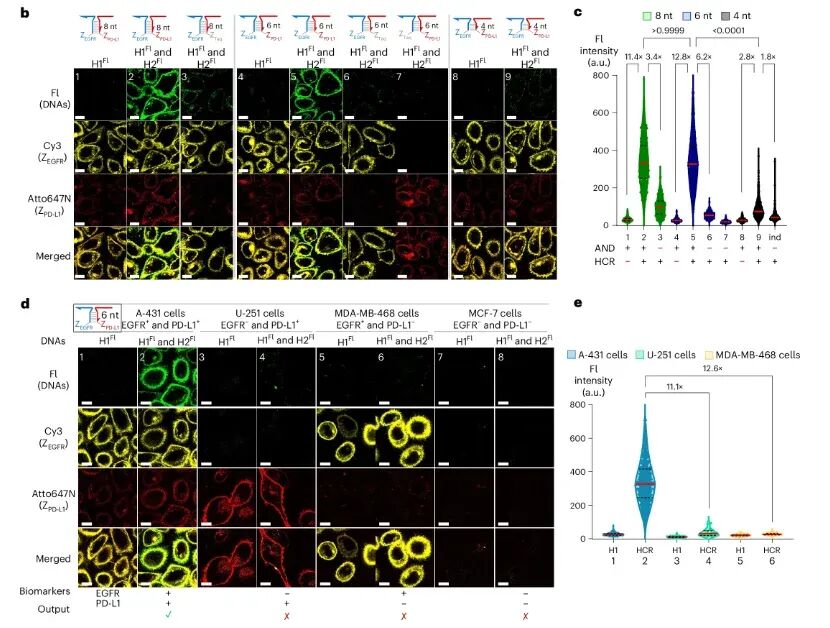
2026 年 3 月27日,《Nature Biotechnology》在线发表了日内瓦大学 Nicolas Winssinger 团队的突破性研究“DNA–drug conjugates enable logic-gated drug delivery amplified by hybridization chain reactions”。他们打造了一套全新的DNA - 药物偶联物(DDC)系统,给抗癌药物装上了可编程的 “逻辑芯片” 和 “信号放大器”,一举突破了当下抗体-药物偶联物(ADC)的核心临床瓶颈,为实体瘤精准治疗、个性化抗癌疗法打开了全新的大门。在癌症靶向治疗领域,ADC素有 “生物导弹” 之称,是当下最热门的抗癌疗法之一。它将能精准识别肿瘤的单克隆抗体、强效杀伤细胞的化疗药物,通过特殊连接子拼接在一起,实现 “精准导航 + 定点爆破”,已经在多种血液肿瘤和实体瘤中取得了临床成功。但风光之下,ADC在实体瘤治疗中始终面临着三大难以突破的痛点:实体瘤穿透能力差:IgG抗体分子量高达150 kDa,难以穿透致密的肿瘤基质,往往只能聚集在肿瘤外围,无法深入瘤体发挥药效;载药量天花板明显:主流的二代ADC仅能携带 2-4 个药物分子,即便是临床大获成功的德曲妥珠单抗,药物抗体比也仅7-8,进一步提升载药量极易影响抗体的靶向性;特异性仍有短板:多数ADC仅依赖单靶点识别,一旦正常细胞低表达该靶点,就可能被误伤,带来不可避免的毒副作用。DDC+HCR:给抗癌药装上 “双密码锁”+“超级放大器”研究团队跳出了传统 ADC 的框架,将 DNA 纳米技术的可编程性、亲和体 / 适配体的精准靶向性,与杂交链式反应(HCR)的信号放大能力完美结合,打造了一套逻辑门控的 DNA - 药物偶联物递送系统。这套系统就像一台精密的 “抗癌智能计算机”,核心分为三大模块,每一步都实现了对传统 ADC 的颠覆:团队放弃了传统的大分子量抗体,转而选用亲和体(<10 kDa) 和核酸适配体作为靶向元件。它们的分子量仅为抗体的 1/15,却保留了不输抗体的高亲和力和特异性,能轻松穿透肿瘤基质,从根源上解决了实体瘤渗透难的问题。2. 双靶点 “AND 逻辑门”,只认肿瘤细胞的 “双密码锁”这是这套系统最精妙的设计之一。研究人员将触发后续反应的 HCR 启动子拆成了两半,分别连接在靶向两种不同肿瘤生物标志物(如 EGFR、PD-L1、PTK7)的亲和体 / 适配体上。只有当两个肿瘤标志物同时存在于同一个细胞表面时,拆分的两段启动子才会在细胞膜上靠近并组装成完整的启动序列,就像一把需要两把钥匙同时转动的密码锁,只有真正的肿瘤细胞才能解锁后续反应。团队通过实验验证,6 个核苷酸(nt)长度的三向连接结构,能在保证反应效率的同时,实现最低的背景泄露,让 “双密码锁” 的精准度达到了极致。3. HCR 链式反应,超百倍放大的 “药物弹药库”完整的启动子一旦形成,会立刻触发杂交链式反应(HCR):大量携带化疗药物的 DNA 发夹结构,会像滚雪球一样在肿瘤细胞膜上发生链式自组装,形成长链聚合物。这个过程实现了惊人的信号放大:在细胞实验中,这套系统实现了最高 217 倍的扩增效率,相比输入的生物标志物,靶向递送的药物信号放大超 100 倍。更重要的是,每个 DNA 发夹都能携带 1-3 个化疗药物分子,一次 HCR 反应就能在肿瘤细胞表面富集海量药物载荷,彻底打破了传统 ADC 的载药量天花板。当 DNA - 药物长链组装完成后,会被肿瘤细胞高效内吞,在细胞内的溶酶体中,通过组织蛋白酶可切割的连接子释放出化疗药物,完成对肿瘤细胞的精准杀伤。b 图:通过显微成像,比较分裂引发剂中 3WJ 长度(4 nt、6 nt、8 nt)对 A-431 细胞 HCR 性能与特异性的影响。c 图:整合 b 图 9 种条件及额外 1 组条件下各细胞膜荧光强度,统计对应细胞数量与生物学重复数,基于中位数计算倍数,采用 Kruskal–Wallis 检验及双尾 Dunn 事后检验分析 P 值。d 图:检测不同生物标志物组合的癌细胞系中,AND 门控响应的特异性。e 图:整合 d 图 6 种条件下细胞膜荧光强度,标注部分条件未定量原因,统计细胞数、生物学 / 技术重复,统计方法同 c 图这项研究不仅完成了技术原理的验证,更通过多组细胞实验,证明了这套 DDC 系统在临床应用中的巨大潜力,每一项突破都直击当下癌症治疗的痛点:双靶点 AND 逻辑门的设计,让这套系统只对同时表达两种标志物的肿瘤细胞发挥作用。在混合细胞培养实验中,治疗组仅对靶标肿瘤细胞实现了高效杀伤,而共培养的正常细胞增殖完全不受影响,几乎没有出现传统化疗 / ADC 常见的 “旁杀伤效应”,极大降低了治疗的毒副作用。实验发现,携带 3 个 MMAE(经典 ADC 细胞毒药物)的 DNA 发夹,能让 HCR 产物的细胞内吞效率提升 10 倍以上,杀伤效果是单药物分子发夹的 50 倍。这种设计让 “低剂量给药、高药效杀伤” 成为可能,在提升治疗效果的同时,进一步降低了全身毒性。这套系统的模块化设计,让药物递送拥有了无限可能。研究人员在不同的 DNA 发夹上分别偶联了 MMAE 和 Dxd(德曲妥珠单抗的核心药物),成功实现了两种不同化疗药物的联合精准递送。这意味着,未来可以根据患者的肿瘤特征,定制化搭配不同的药物组合,应对肿瘤异质性和化疗耐药性,真正实现 “一人一方” 的个性化抗癌治疗。除了直接递送化疗药物,研究团队还解锁了这套系统的另一大潜力:通过 HCR 反应,在肿瘤细胞表面特异性招募抗体。实验证实,HCR 形成的 DNA 长链能以极高的亲和力捕获抗体,这为抗体依赖的细胞毒性(ADCC)、靶向免疫降解等免疫治疗策略提供了全新平台,让这套系统不止能直接杀伤肿瘤,更能激活患者自身的免疫系统对抗癌症。a,不同荧光素标记(FITC)DNA 组装体的表面等离子体共振(SPR)传感图及结合常数(通过 SPR 测定,将抗 FITC 抗体以低载量固定于 SPR 芯片表面。测试浓度:400 nM 至 12.5 nM,采用两倍梯度稀释)。ND,未测定。b,为获取 c 中所示图像而开展的实验示意图。c,经 ZEGFR-S2 与 ApPTK7-S1 处理,并联合不同发夹结构、单克隆抗体(mAb)及蛋白 G 组合处理的 A-431 细胞显微图像。d,c 中 DyLight 405(蛋白 G)的积分荧光强度(从左至右细胞数 n 分别为 195、367、320、363、351 和 290;数据分别来自 3、5、5、5、5 和 4 次技术重复)。比例尺为 10 µm;每个发夹结构在 5' 端均连接一个荧光素分子。合并通道:DyLight 405、荧光素(Fl)、Cy3 与 Atto647N / 细胞膜深红色染料的叠加图像。当然,这项研究目前仍处于细胞实验阶段,走向临床还需要解决一些挑战:比如未修饰的 DNA 在血浆中代谢稳定性不足,团队也指出,未来可通过镜像 DNA(L-DNA)、化学修饰的适配体等方式,轻松解决这一问题。而相比传统 ADC 依赖蛋白表达的生产模式,这套 DDC 系统完全基于化学合成,能实现对药物偶联位点、数量的精准控制,批次间稳定性更高,纯化和质控流程更简单,为后续的临床转化和规模化生产打下了坚实的基础。推文用于传递知识,如因版权等有疑问,请于本文刊发30日内联系医药速览。
内容中包含的图片若涉及版权问题,请及时与我们联系删除










评论
沙发等你来抢