2026年3月17日,杜克大学法学院的Arti K. Rai与波士顿大学法学院的Janet Freilich在《Nature Biotechnology》上发表文章,题为“Patents on AI-derived drugs: empirical evidence and legal challenges”。

背景
计算机辅助药物发现已有数十年历史,但人工智能技术的加速应用正带来变革性潜力。从识别新靶点、预测蛋白质折叠,到虚拟筛选药物-靶点相互作用,再到设计和合成具有良好药理学特性的小分子,AI正在渗透药物发现的每一个环节。初步成果包括临床前阶段的速度提升和成本降低,部分分子在I期试验中显示出更低的毒性。支持者还希望AI生成的药物能更具创新性,结合新靶点或采用与已知药物截然不同的化学结构,从而满足未获满足的治疗需求。
然而,药物研究的漫长孕育期意味着,关于AI应用影响的有力、公开证据才刚刚开始出现。尽管已有数十种AI生成的药物进入临床试验,但尚未有任何AI发现的药物获得批准。在这一不确定的背景下,专利数据提供了一扇独特的观察窗口——由于专利通常在药物进入临床试验前几年就已提交,可供研究的专利公开总数远多于临床阶段的药物数量。
基于此,作者考察了AI生成药物的科学独特性及其引发的法律挑战。研究团队从市场研究数据库Pitchbook中识别出116家主要依赖AI开发药物的公司(“AI原生”公司),并收集了这些公司在2014–2023年间提交的小分子化合物专利及专利申请(共153项),同时按照提交年份、发明人公司规模及专利律所等维度,匹配了153项传统方法开发的对照专利。通过比较两组专利在靶点独特性、结构独特性以及靶点-结构组合独特性三个维度的差异,该研究得出了若干重要发现。
靶点独特性:聚焦明确,但并非更独特
AI原生公司是否更倾向于靶点驱动的药物发现?答案是肯定的。数据显示,AI原生公司有80%的专利在标题中明确指定了治疗靶点,而对照公司这一比例仅为63%,差异具有统计学显著性(P=0.002)。这印证了AI原生公司更侧重基于靶点的发现策略。
然而,聚焦靶点并不意味着靶点更具独特性。研究团队通过DrugBank数据库(涵盖约17,000种已批准和实验性药物)统计了每项专利所针对靶点在此前已有多少临床资产。结果显示,AI原生公司专利中分子所针对的靶点,此前平均有22个临床资产(中位数3个)以之为靶点;而对照组平均为9个(中位数3个),差异不显著(P=0.28和P=0.97)(图1a)。换言之,AI原生公司选择的靶点并不比传统公司更“冷门”。从治疗领域看,AI原生专利中最常见的是癌症(占80%),与对照组(70%)无显著差异。
值得关注的是时间趋势和临床阶段差异。在样本早期年份(2014-2016年左右),AI原生公司药物的靶点独特性显著高于对照组;但随后对照公司的靶点变得越来越独特——大约每年减少1个具有相同靶点的化合物(P=0.03)。这可能反映了传统药企也开始融入AI技术,或者它们有意转向更独特的靶点。此外,样本中已进入临床试验的AI生成化合物,其靶点反而比未进入临床的AI化合物更“常见”(中位数46个共享化合物vs.13个),提示更独特的靶点可能伴随着更高的临床失败风险,或者这些独特的候选药物尚处于更早期的开发阶段。
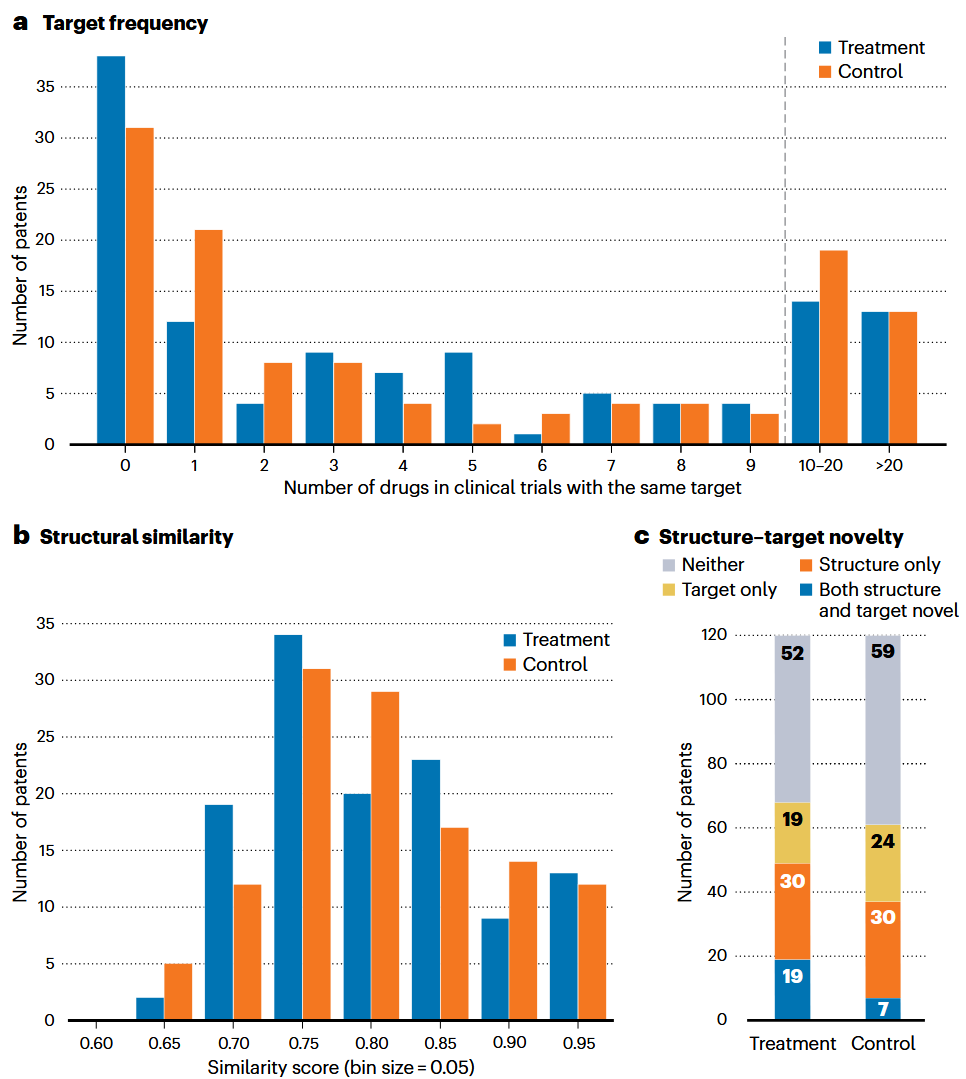
图1 对AI原生公司提交的专利(处理组)与匹配的非AI生成专利(对照组)从三个维度进行科学独特性分析:靶点独特性、结构独特性以及靶点-结构组合独特性。
结构独特性:与已知分子高度相似,但与现有药物差异显著
结构独特性是衡量药物创新性的另一核心指标。研究使用CAS SciFinder数据库(涵盖约2.75亿种物质)的专有相似性度量,计算每个先导化合物与优先权日前已披露的最相似分子之间的相似度。结果发现,AI生成药物的中位数相似度为83%(四分位距77–89%),与对照组的84%(78–90%)几乎相同(图1b)。在药物开发中,70–80%的相似度通常被认为具有高度相似性——这意味着绝大多数新专利化合物(无论是否由AI生成)与已知化合物整体相比,并不特别独特。
然而,当比较对象缩小为DrugBank数据库中已进入临床试验的现有药物时,情况发生了显著变化。AI生成药物与最相似的临床药物之间的中位数相似度仅为27%(四分位距24–32%),对照组同样为27%(24–31%)。这表明,无论是AI生成还是传统方法发现的候选药物,在结构上都与已经获批或进入临床试验的药物存在较大差异——它们并非简单模仿现有药物,而是在探索新的化学空间。
研究还识别出12个由AI原生公司原创开发、已公开结构且进入临床试验的资产,其结构独特性指标与对照公司的临床资产无显著差异。换言之,AI并未在结构独特性上带来超越传统方法的系统性优势。
组合独特性:AI的潜在优势领域
尽管在单独的靶点或结构维度上,AI生成药物并未表现出显著优势,但当两个维度结合时,差异浮现出来。研究将“独特靶点”定义为没有其他处于临床试验中的药物针对同一靶点,将“独特结构”定义为在CAS SciFinder中没有结构相似度达到0.8或以上的已知化合物。结果显示,AI原生公司中有19种化合物(12%)同时具备靶点独特性和结构独特性,而对照化合物中仅有7种(5%),差异显著(P=0.03)。
这一发现具有重要的科学和临床意义。同时具备新靶点和新结构的化合物最有可能成为“首创药物”(first-in-class),这类药物能够针对全新的生物学机制,满足现有疗法无法覆盖的医疗需求。尽管从新颖性到临床获益还有很长的路要走,但这一信号表明,AI工具有望帮助研究人员跳出既有框架,探索更具颠覆性的药物组合。
法律挑战:AI对专利制度的三大冲击
专利不仅是科学数据的载体,也是法律争议的焦点。该研究进一步分析了AI使用在专利法层面引发的三个核心问题。
专利有效性的核心要求之一是“非显而易见性”。对于结构高度相似的分子,申请人必须证明其具有意想不到的性质。虽然AI生成药物的中位数相似度(83%)提示其与现有分子高度接近,但对照组同样如此。因此从结构上看,AI专利并不比传统专利更容易受到显而易见性质疑。真正的挑战来自发现过程。美国专利法第103条明确规定,发明是否显而易见不应取决于发明的方法。然而,如果普通药物化学家能够使用公开可用的AI系统轻易地识别出某个分子结构,该结构就可能被认定为显而易见。随着AI工具日益普及和强大,这一风险将不断放大。
2022年,美国联邦巡回法院在Thaler v. Vidal案中裁定,现行专利法不允许将AI系统列为发明人。这引发了一个棘手的问题:在AI辅助下,需要多少人类贡献才能将一个人列为有效发明人?这一问题在美国尤其尖锐,因为宪法将专利授予“发明人”,而最高法院的原旨主义解释倾向于将“发明人”限定为人类。拜登政府时期,美国专利商标局曾发布指导性案例,列举了药物开发中足以表明人类发明人资格的贡献水平。然而,2025年11月,特朗普政府废除了这一指南,转而采用更简略的表述:所有专利的主题必须由人类发明。这一政策变化并未解决量化问题,反而增加了不确定性。
美国专利法不要求实际制造出发明物,AI的输出本身可能足以提交专利申请。这加剧了已有的“早期申请”倾向,在药物发现的最早期阶段就抢占专利优先权。过早地将专利权分配给那些不具备商业化能力的实体(如小型AI初创公司),可能会损害那些更有能力完成临床试验、监管审批和市场推广的企业的专利保护和商业化能力。研究建议,提高专利审查中的证据门槛可能有助于缓解这一担忧。更严格的要求(例如需要提供初步的实验验证数据)不仅能够筛选出更成熟的发明,还能通过增加人类努力投入,间接证明非显而易见性和人类发明人资格。
总结
总体而言,这项实证研究传递了两个层次的信息。在科学层面,AI生成药物目前并未在靶点或结构独特性上显著优于传统方法,但在靶点-结构组合创新方面展现出初步优势。此外,AI原生公司的临床前化合物比临床化合物具有更独特的靶点,暗示未来可能有更多创新疗法进入管线。在法律层面,AI使用并未使现有专利体系立即失效,AI药物的结构独特性与对照相当,因此非显而易见性挑战并非更严重。但AI的确提出了三个根本性问题:当发现过程变得“显而易见”时如何维持专利有效性;人类发明人资格需要多少贡献;以及如何防止过早申请损害整体创新效率。
如果AI工具最终使突破性药物的发现变得廉价、快速且无需大量人类投入,那么专利制度的基本经济学理由—激励那些容易被廉价复制的昂贵创新—也将变得模糊。届时,药物开发中真正昂贵的部分可能仅限于人体临床试验,而所需的激励可以通过临床试验数据独占期来提供。AI尚未从根本上改变获得专利的药物,但它已经对专利法发出了预警。如果AI真能实现其彻底改变药物开发的承诺,我们可能需要重新思考专利制度在创新生态中的角色与边界。
参考链接:
https://doi.org/10.1038/s41587-026-03039-x
--------- End ---------

内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢