期刊:PNAS
DOI: 10.1073/pnas.2602101123
前言
努南综合征(Noonan syndrome, NS)是MAPK通路过度激活引起的最常见RAS通路病,患者常伴有肥厚型心肌病等严重并发症,其中约8%的病例由CRAF激酶突变导致。
正常情况下,CRAF激酶通过S259位点的磷酸化与14-3-3蛋白结合,形成抑制性复合物,使CRAF维持自关闭状态。但在努南综合征中,CRAF基因突变会导致S259磷酸化程度降低和/或改变与14-3-3蛋白结合的序列,破坏这一复合物结构,使CRAF异常激活且下游ERK信号增强。目前临床仅能使用MEK抑制剂曲美替尼对症治疗,缺乏针对病因的特异性药物,且长期使用副作用明显。
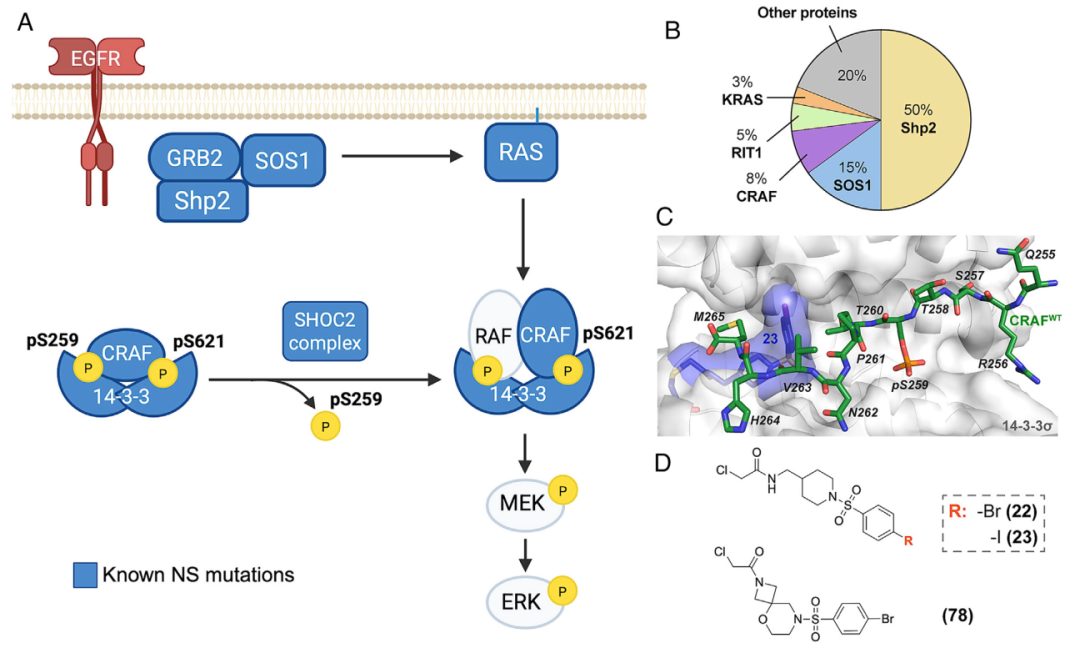
图1. 14-3-3/CRAF-pS259复合物作为努南综合征的治疗靶点
近年来,能够选择性稳定蛋白质-蛋白质相互作用的分子胶药物为修复被突变削弱的复合物提供了新思路。研究团队前期已开发出能稳定14-3-3σ与正常CRAF结合的共价分子胶。那么,这些分子胶能否同样修复被突变削弱的14-3-3/CRAF复合物,从而抑制过度激活的信号通路呢?
近日,加州大学Michelle R. Arkin等研发人员首次证实,分子胶药物可以修复努南综合征(NS)中基因突变造成的蛋白相互作用缺陷,恢复MAPK通路稳态。研究为NS等RAS通路病的治疗提供了一种全新策略。
相关研究以“Restoring the 14-3-3/CRAF regulatory interaction in Noonan syndrome using molecular glues”为题,4月28日在线发表于《PNAS》上。

研究内容
分子胶药物增强上游NS突变背景下的CRAF-pS259磷酸化
为评估稳定14-3-3σ/CRAFWT调控相互作用对NS的调控效果,研究者首先在上游NS突变(Shp2、SOS1、SHOC2突变)背景下测试了分子胶化合物23的效果。结果显示,尽管这些上游突变对基础pS259水平影响有限,化合物23仍能使所有突变背景下的pS259增加至少1.5倍;对于增强pS259去磷酸化酶活性的SHOC2S2G突变,化合物23更是将其恢复至超过野生型基础水平。
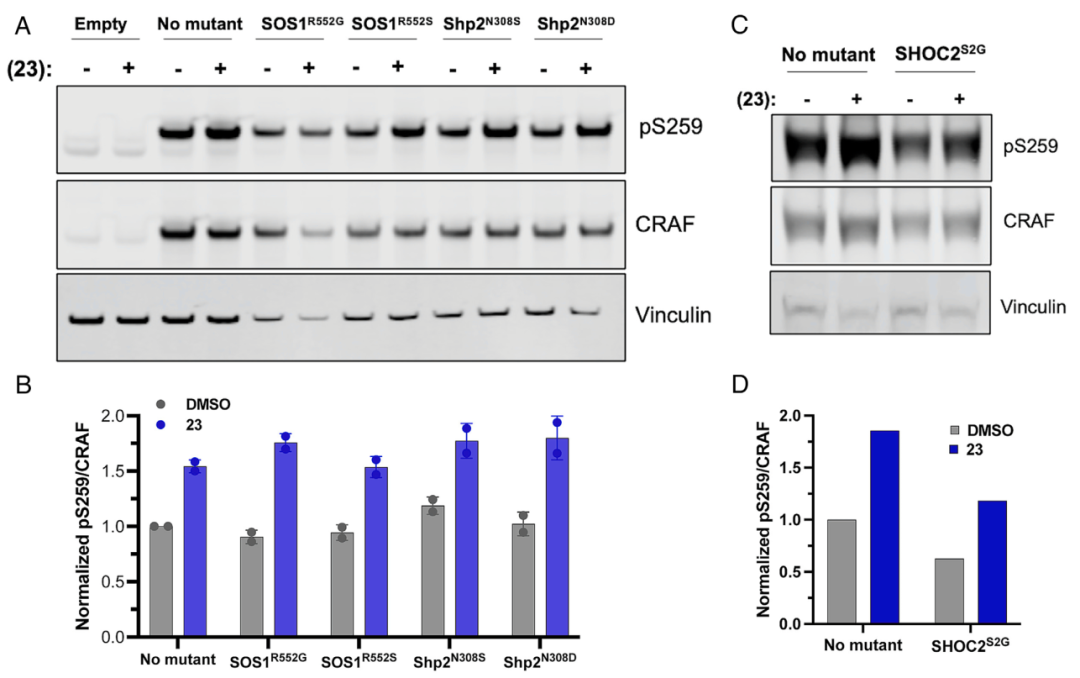
图2. 上游NS突变背景下CRAF-pS259磷酸化保护
CRAF NS突变直接损害14-3-3/CRAF调控相互作用
CRAF致病突变会大幅降低与14-3-3的结合亲和力,并减少S259磷酸化修饰。这些改变直接解除CRAF自抑制,导致下游 ERK 通路过度激活。
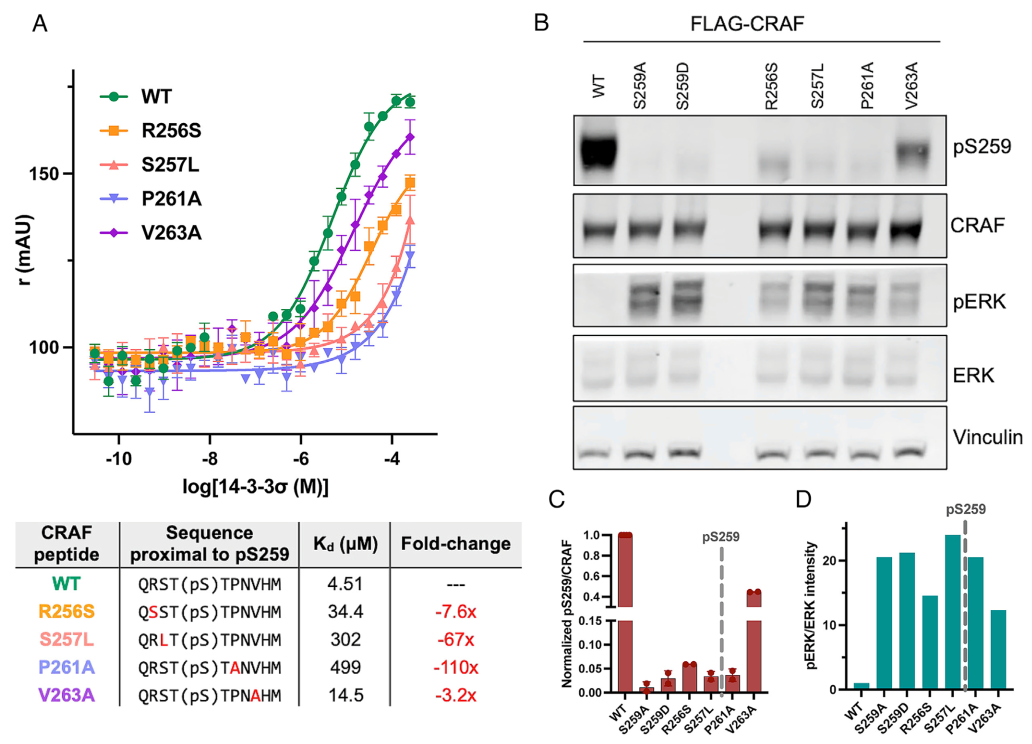
图3. CRAF突变对结合亲和力和磷酸化的影响
分子胶药物恢复14-3-3σ/CRAFNS蛋白/肽段复合物
团队在生化水平证实分子胶可修复被突变削弱的 14-3-3/CRAF 相互作用。分子胶化合物22、23、78 均能显著提升突变体多肽与14-3-3σ 的结合能力,其中23对S257L 和V263A 的修复效果最为突出,晶体结构也显示分子胶可弥补突变带来的构象偏差,稳定结合界面。
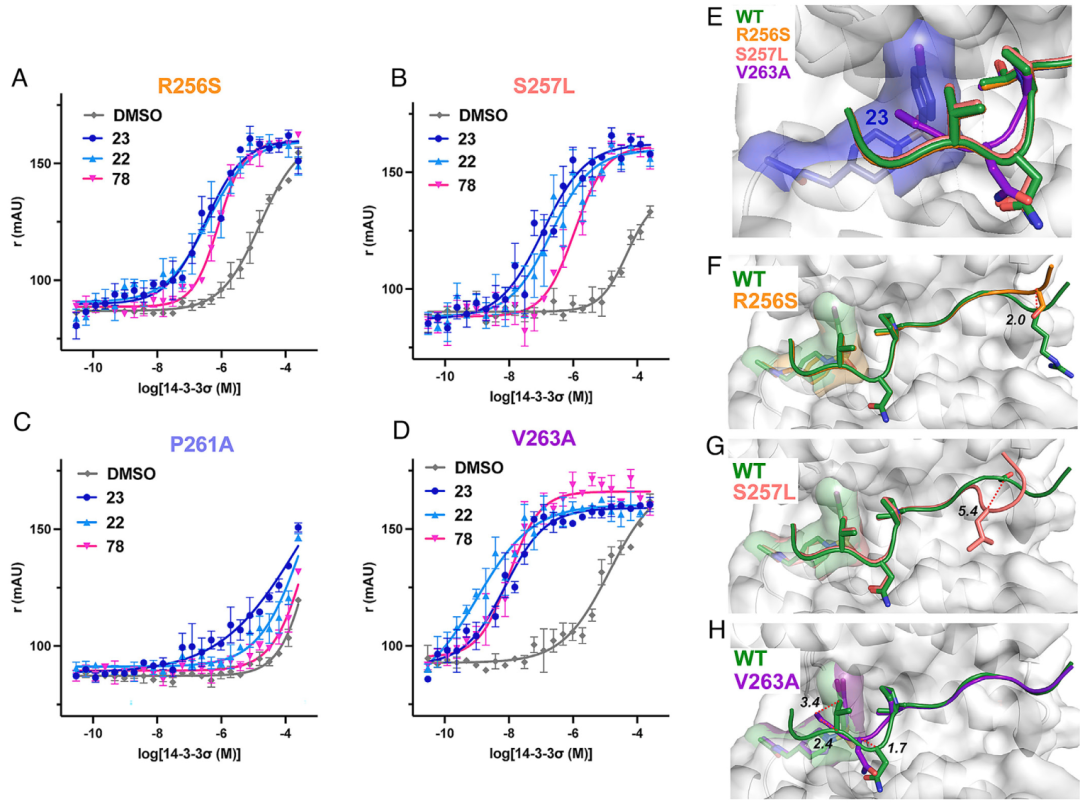
图4. 14-3-3σ/CRAFNS蛋白-肽复合物的生化稳定性
分子胶药物在细胞内恢复 14-3-3 与 CRAFNS的相互作用
NanoBRET 与Western blot 证实,分子胶可恢复全长突变CRAF与14-3-3σ 的结合,同时提升pS259 磷酸化水平;这些作用依赖于14-3-3σ的C38位点,具有高度特异性。
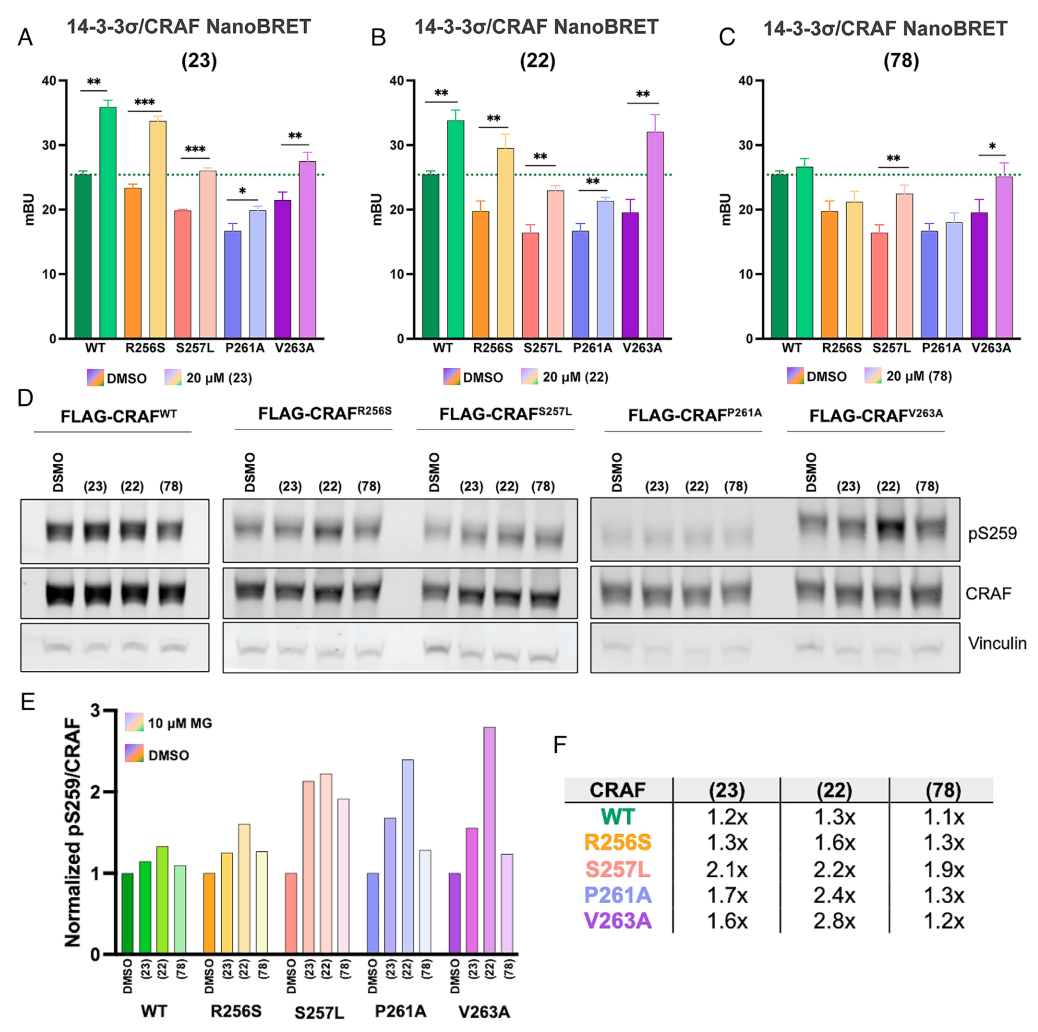
图5. 细胞中14-3-3σ/CRAF的分子胶稳定性
分子胶药物抑制CRAF激酶激活机制
分子胶通过稳定14-3-3/CRAF抑制复合物,阻断CRAF与RAS的结合及二聚化,最终下调pERK。分子胶23对ERK的抑制效果与现有MEK抑制剂曲美替尼效果相当。
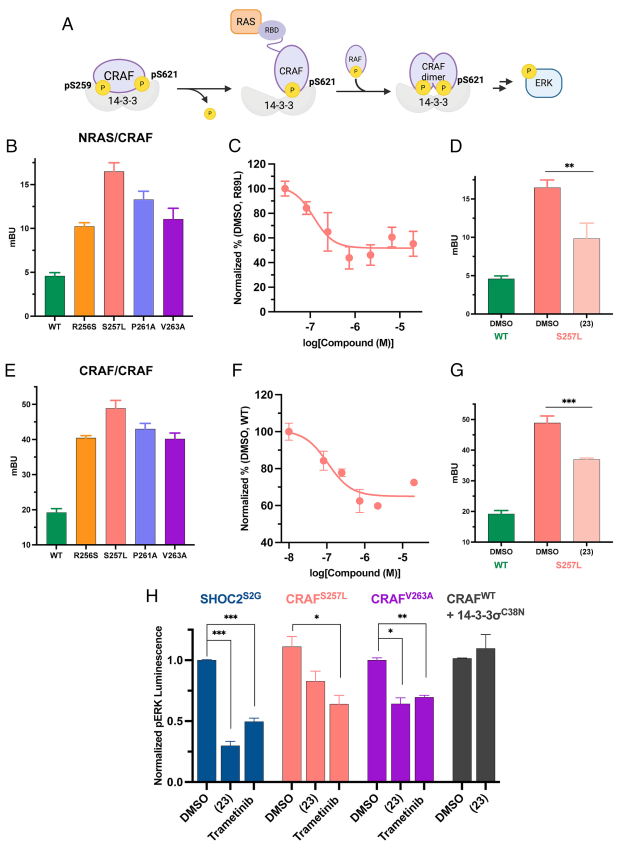
图6. 分子胶通过稳定14-3-3σ/CRAFNS抑制CRAF激酶活化
总结
本研究首次证实,靶向 14-3-3σ/CRAF 的分子胶能够有效修复努南综合征突变所削弱的抑制性蛋白相互作用,通过稳定 CRAF S259 磷酸化、阻断CRAF 与RAS 结合及二聚体形成,显著下调异常激活的MAPK 通路,效果与临床药物曲美替尼相当,为治疗提供了全新的机制与方向。
这项工作不仅验证了分子胶在修复致病突变破坏的蛋白复合物方面的可行性,也为努南综合征及其他 RASopathy 疾病提供了精准调控MAPK通路活性的治疗新思路,未来有望进一步优化分子胶结构、拓展适用突变类型,并向临床转化,最终填补这类疾病特异性疗法的空白。
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢