2026年5月8日,中国衰老标志物研究联合体(Aging Biomarker Consortium, ABC)在Cell Press细胞出版社旗下期刊Cell发表题为“Multimodal clocks of human aging”的研究论文。研究团队建立了一个可量化、可模拟、可干预的“衰老数字人体”框架,通过整合多维度、多中心标准化数据,构建了多层次、可解释的衰老时钟体系,实现对个体生物学年龄的精准评估和器官衰老异质性的解析。
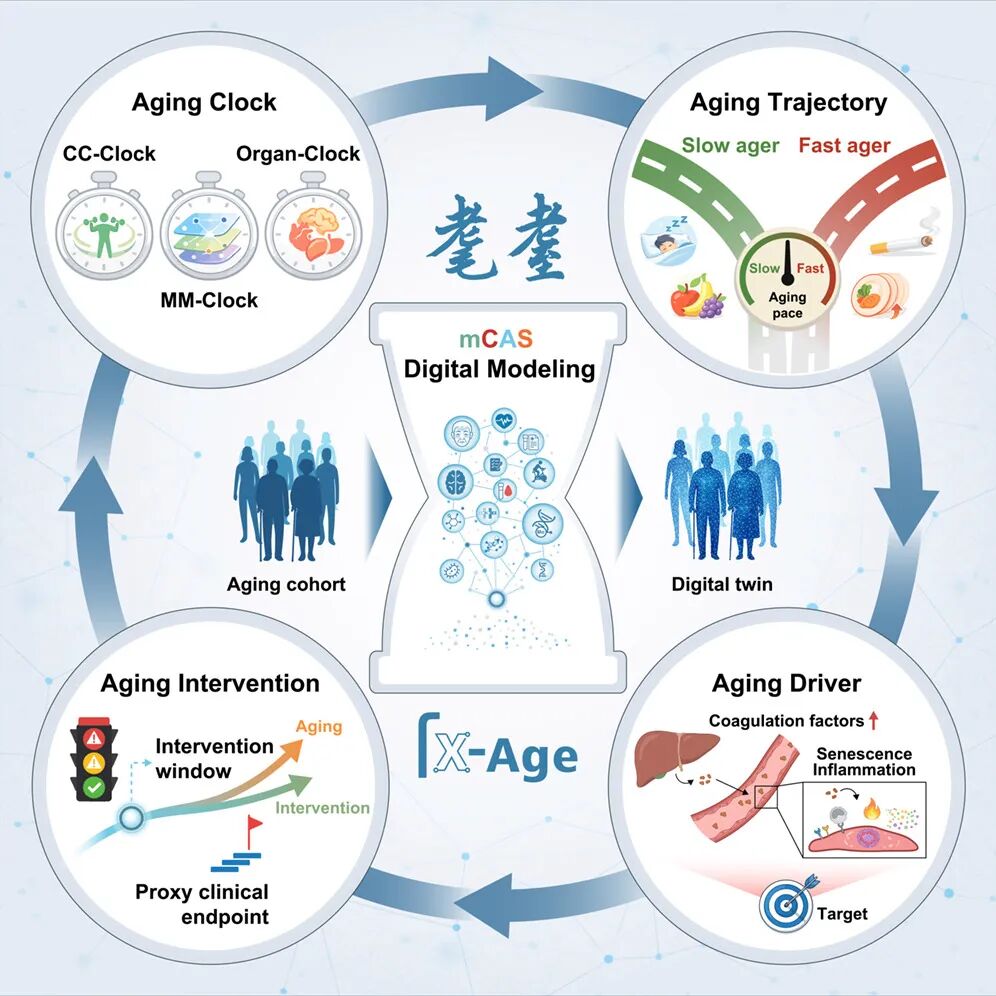
衰老研究长期面临一个根本性挑战,即描述性发现远多于因果性理解,关联性标记难以转化为干预靶点。要突破这一瓶颈,不仅需要回答一个人有多老,更需要明确哪里先老、为何而老以及如何干预。该研究基于覆盖2019名18至91岁健康个体的四中心标准化队列,整合240余项临床生理参数及多层次分子表型数据,包括甲基化、转录组、蛋白质组、代谢组、宏基因组和单细胞转录组,构建了三个功能互补的衰老时钟模块。核心能力时钟刻画整体生理功能的衰退轨迹。多模态时钟通过深度学习融合多层级数据,将生物学年龄预测的平均绝对误差降至3.87年。器官特异性时钟依托液相活检策略,独立评估脑、肝、肺、肌肉、血管、皮肤六个器官的生物学年龄,揭示肝脏衰老拐点约为40岁,显著早于大脑的约50岁,并识别出40至50岁和60至70岁两个衰老加速的非线性窗口。
该研究进一步从关联走向因果。多个凝血因子在衰老进程中协同上调,其主要来源为衰老的肝脏。体外实验表明,这些凝血因子可直接诱导人主动脉内皮细胞发生衰老表型。体内实验证实,注射凝血因子F13B可诱发小鼠多组织加速性衰老。这些证据表明,血浆中累积的特定凝血因子是驱动血管及多器官衰老的功能性分子。
在临床转化层面,约100个血浆蛋白即可高效重建核心能力时钟和器官时钟,提示常规血检有望成为评估生物学年龄的可行路径。器官特异性衰老时钟可提前识别超前老化的器官,为早筛早诊提供更早的时间窗口。生活方式分析显示,较早入睡、适量步行及规律摄入水果与生物学年龄减速显著相关。此外,研究还识别出多个与衰老相关疾病存在因果关系的蛋白,为药物靶点发现提供了新方向。
该工作标志着衰老研究从碎片化、描述性向标准化、系统性和因果性的范式转变,提出可量化的生物学年龄作为衰老干预的临床终点参考,系统回答了一个人老得多快、哪个器官先老、为何而老以及从何处干预这一系列核心问题。
Cell Press细胞出版社特别邀请论文通讯作者刘光慧研究员进行专访,请他为大家做进一步的深入解读。
CellPress:
这项研究的起点是什么?希望解决什么科学问题?
研究的起点是一个根本性的医学问题:能否像测量血压一样,系统、定量地评估一个人的健康衰老程度?
长期以来,衰老研究面临一个困境。描述性发现远多于因果性理解,关联性标记难以转化为干预靶点。研究往往聚焦于单一分子或某条信号通路,每个视角都反映了真实的局部,却难以整合成完整的个体化健康模型。
核心科学问题可以拆解为三个递进的层次。第一,一个人的身体整体上老得有多快?第二,哪个器官在健康上率先掉队?第三,是什么在驱动这种异步老化?只有回答了这三个问题,衰老才有可能从模糊的概念转变为可操作、可追踪的临床健康终点。
CellPress:
为什么要构建“衰老数字人体”?它能解决传统方法解决不了的问题吗?
衰老本质上是一个多系统相互作用的复杂网络。没有系统性的刻画,就无法知道从何入手干预。因此,将衰老的宏观结构以数字化的方式呈现,是理解它、干预它的前提。
这一框架的价值在于从整体到局部的定位能力。先通过数字模型定位衰老加速的器官或系统,再追问内部发生了什么、哪些分子在驱动。这是一个从宏观定位到微观解析并行的研究路径。
在技术路线上,重点在于面向人类应用的无创性和可转化性。血浆蛋白检测在临床上已比较成熟,适合体检中心和社区场景。通过人工智能对数据的整合学习,仅需外周血的特定蛋白组合,就能以数字化方式评估个体的生物学年龄和器官状态。这种液相活检结合数字建模,让衰老评估有机会真正走出实验室。
在宏观层面,器官衰老存在显著的异步性。肝脏的衰老拐点约为40岁,早于大脑的50岁,提示代谢器官对早期衰老更为敏感。研究还识别出40至50岁和60至70岁两个非线性加速窗口,后者伴随血压升高、骨密度下降及凝血通路的显著激活。这使得同一个体的器官异步性首次得以定量呈现。
在分子层面,凝血因子被锁定为一个关键的因果驱动分子。传统上,凝血因子被认为主要参与血栓形成,其与衰老的关联多被解释为老年人群心血管事件风险增加的伴随现象。多模态时钟注意到,多个凝血因子在老年个体中获得极高的注意力权重。进一步追踪发现,这些因子主要来源于衰老的肝脏。体外实验证实,凝血因子可直接诱导人类血管内皮细胞衰老。体内实验则证明,注射上调的凝血因子F13B可诱发小鼠多组织的加速衰老和免疫炎症浸润。
这些结果指向一个潜在的机制链条。衰老肝脏合成的凝血因子在血浆中异常累积,攻击血管细胞,诱导其进入衰老状态,进而通过炎性扩散波及多个器官。凝血因子不是衰老的“乘客”,而是“司机”之一。这一发现为临床提供了新的思路。监测血浆凝血因子水平或可用于评估生物学年龄,靶向特定凝血因子则可能成为延缓衰老的新策略。
CellPress:
与传统衰老时钟相比,“衰老数字人体”有哪些实质性进步?
传统的衰老时钟,如基于DNA甲基化的模型,本质上是一个年龄计数器,根据分子特征预测时序年龄,回答的是出生了多少年。但同样年龄的两个人,生物学状态可能天差地别。
这一框架的优势体现在三个方面。第一,从预测时序年龄转向评估功能状态。关心的不止是分子读数,更是器官的真实工作能力,这是临床真正需要的。第二,传统时钟只能给出一个整体的年龄估值,而这一框架可以明确哪个器官先老化、老化得多快。第三,多数时钟提供的是相关性标记,这里筛选出的信号能指向可干预的靶点。
在服务临床方面,这项研究基于中国人群的标准化多中心队列,通过统一标准让不同中心的数据可比。未来,或许常规血检即可评估个体的器官衰老状态,识别加速老化的器官,为早筛早诊和个性化干预提供依据。
CellPress:
下一步的研究方向是什么?主要挑战在哪里?
当前研究基于横断面数据,能反映群体层面的衰老差异,但无法揭示个体的动态衰老轨迹,也看不到从健康到疾病的演化过程。ABC正在建立的前瞻性队列,将对同一批参与者长期追踪,为个体化预测和疾病转化路径的绘制奠定基础。
从因果发现到临床转化,凝血因子这条路径仍需系统评估。下一步需要开发特异性抑制剂,在更接近人类的模型中评估安全性和有效性。研究发现了两个衰老加速窗口,但何时介入最有效、不同器官是否需要不同策略,尚不清楚。这是决定衰老干预能否落地的关键问题。
此外,还需要降低技术门槛,让衰老评估走出实验室,进入体检中心和家庭。目前正在探索干血斑检测或可穿戴设备等低成本方案。
挑战来自技术和理念两个层面。技术上,检测的精准性、敏感性和便捷性仍有提升空间。理念上,衰老能否被视为可测量、可干预的过程,监管机构能否接受“生物学年龄”作为临床终点,这是全球衰老研究的共同命题。随着“衰老数字人体”的不断迭代,希望最终能够实现从“治已病”到“防未老”的转变。
ABC成立于2022年,由衰老生物学、老年医学及交叉学科领域的研究人员组成,聚焦人类衰老标志物的发现与临床转化。联合体已在《细胞》、《自然·医学》、《自然·衰老》、《自然综述·分子细胞生物学》等期刊发表系列研究成果,发布了覆盖脑、心脏、骨骼、血管、肝脏、脂肪、骨骼肌、听觉系统、视觉系统等多个器官系统的衰老标志物专家共识,初步构建了从标志物框架到临床应用的研究链条。由联合体牵头实施的X-Age项目(“耄耋”计划)已完成“耄耋1.0”框架的搭建,为衰老研究的标准化和国际化提供了技术支撑。
论文原文刊载于Cell Press细胞出版社旗下期刊Cell,
点击“阅读原文”或扫描下方二维码查看论文
Multimodal clocks of human aging
https://www.sciencedirect.com/science/article/abs/pii/S0092867426004605
https://doi.org/10.1016/j.cell.2026.04.025
内容中包含的图片若涉及版权问题,请及时与我们联系删除

























评论
沙发等你来抢