
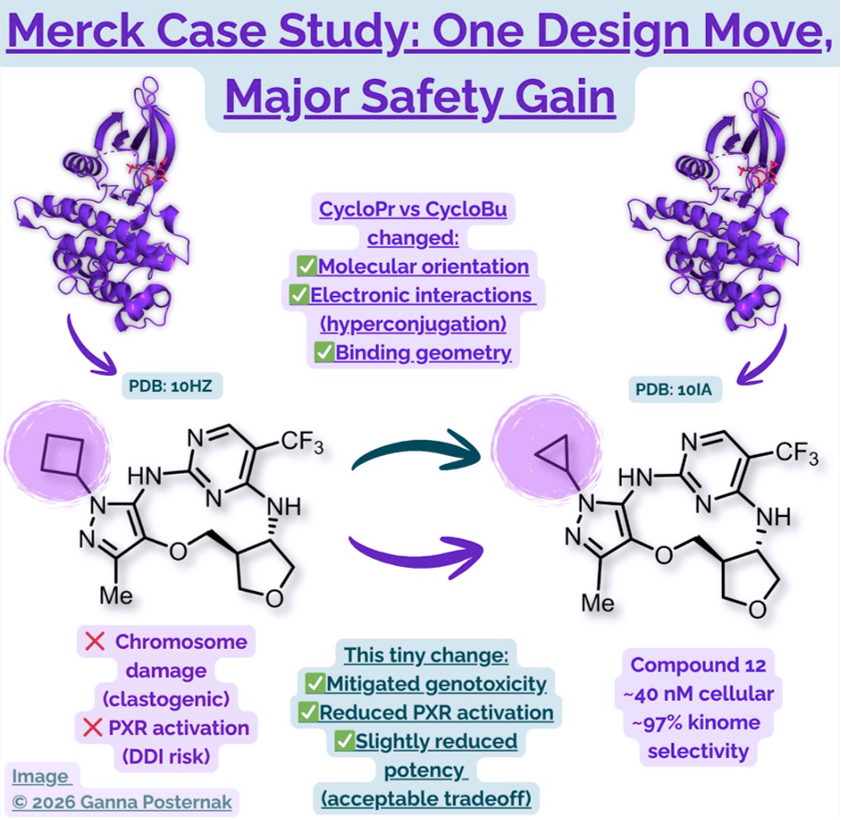
🔍默克公司聚焦于靶向 LRRK2 激酶开发帕金森病全新治疗药物,LRRK2 激酶与病情进展密切相关,优化所得的 先导化合物12 为首个非遗传毒性、低剂量、脑穿透大环 LRRK2 抑制剂。
DOI: 10.1021/acs.jmedchem.6c00238

大环化技术与迭代药物设计策略
对化合物进行大环化及结构优化,力求同时满足高活性、高选择性及中枢神经系统穿透性这一极具挑战性的多重成药要求。
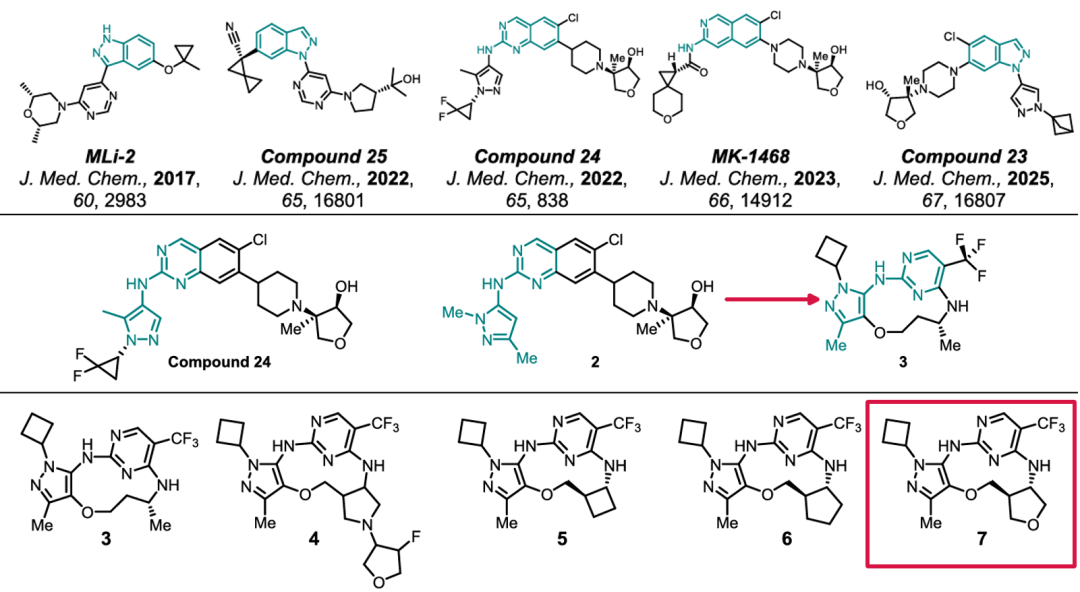
骨架优化
👉 该化合物的遗传毒性,并非源于靶向抑制 LRRK2 的作用机制,而是由抑制 TTK 等特定脱靶激酶所导致。
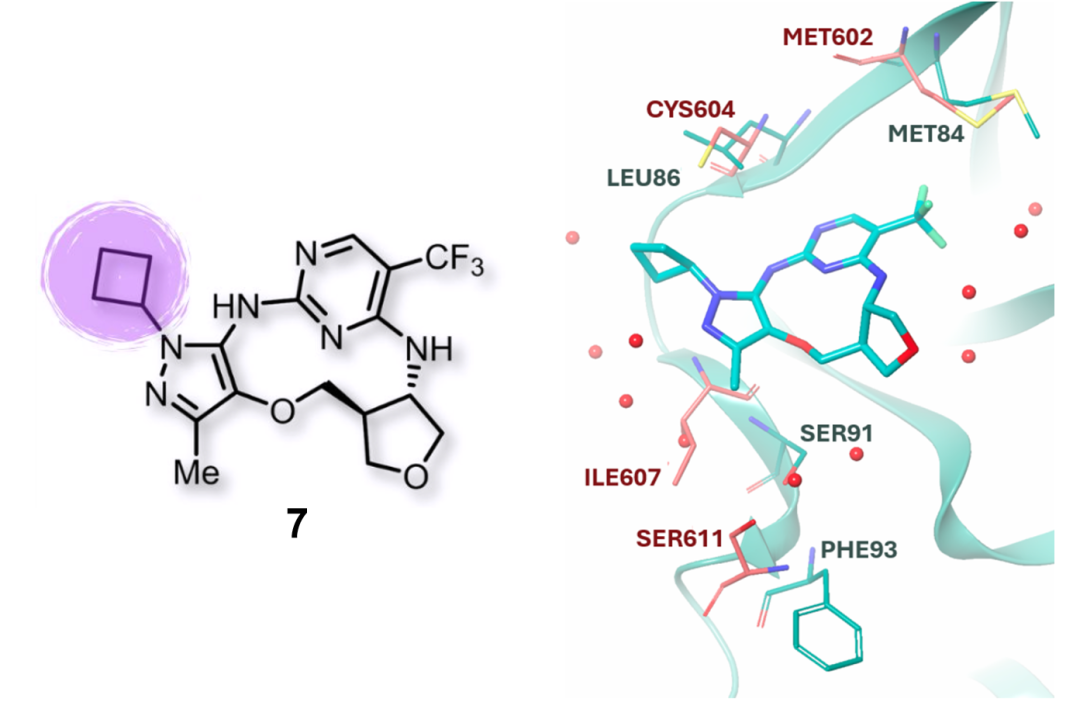
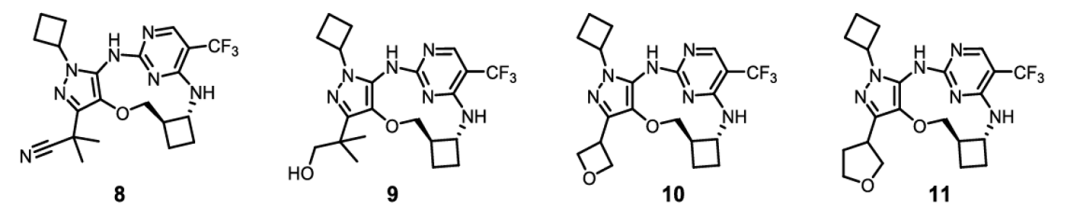
🎯关键性突破分子骨架的细微改造:将环丁基替换为环丙基。
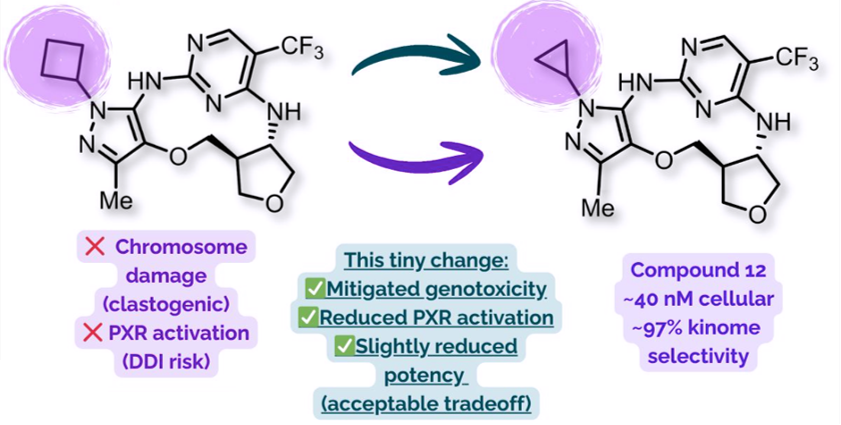
大环化优势:降低EPSA/tPSA,掩蔽极性,降低 P-gp 外排,提升 CNS 可达性。
构效关系:铰链区环丙基的空间取向与超共轭效应,降低亲脂性、减弱 PXR、消除遗传毒性。
临床价值:化合物12为首个非遗传毒性、低剂量、脑穿透大环 LRRK2 抑制剂,可作为体内工具分子验证 LRRK2 靶向治疗帕金森病。
合成路线
⚖️ 最终得到一款综合成药性质更均衡的全新先导化合物。合成路线见下:
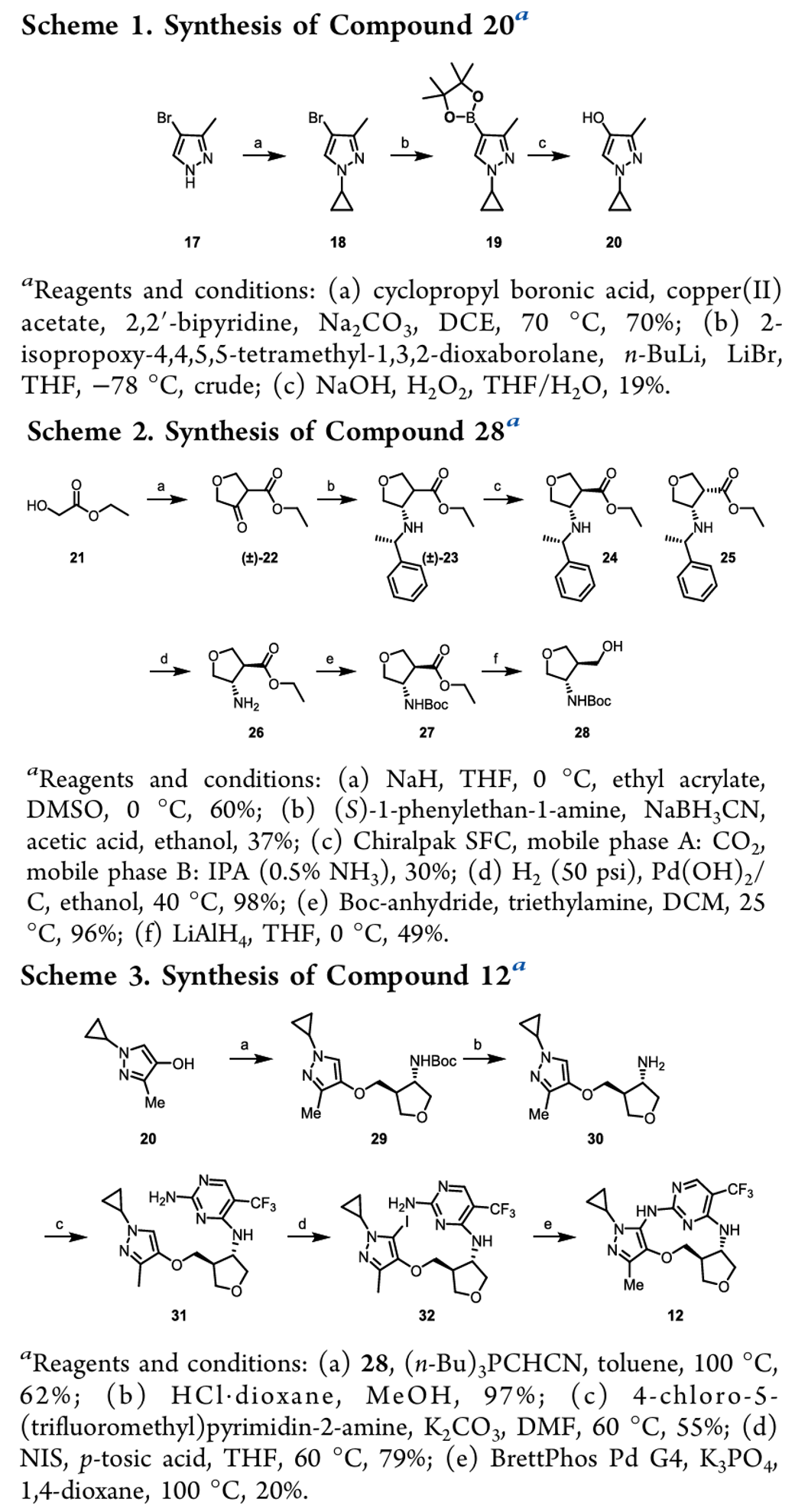
总结
这一案例充分说明,基于作用机制的药物设计,能够帮助研发人员平衡并攻克多重相互制约的成药难题:陷入瓶颈的药物研发项目,依靠对问题的深度剖析和精准的结构设计决策实现翻盘,而非单纯依靠反复试错迭代。
内容中包含的图片若涉及版权问题,请及时与我们联系删除



评论
沙发等你来抢